quimico
2013-04-29 20:26
Gli alogenuri di boro sono utili reagenti in chimica organica. Tra di essi, il tribromuro di boro deve essere messo in luce, a causa delle diverse reazioni che può fare, come la scissione di eteri, amine, e tioli, e l'addizione ad alleni ed alchini. Questi sono molti esempi del suo uso in medicinal chemistry, nella sintesi di prodotti naturali, e nello sviluppo di nuovi materiali organici.
BBr3 è un liquido incolore, che fuma all'aria. È commercialmente disponibile tal quale o in soluzione di diclorometano o esani o come complesso, ad esempio dimetilsolfuro complesso.
Precauzioni: BBr3 è estremamente sensibile all'umidità e si decompone all'aria con sviluppo copioso di HBr. DEVE essere conservato sotto atmosfera inerte anidra. Reagisce violentemente con i solventi protici come acqua ed alcoli; anche gli eteri sono solventi inappropriati.
La sintesi di tale composto non è facile, neanche per i più esperti, come avrete capito dalla presentazione di tale composto.
La sintesi storica prevedeva la reazione del triossido di boro con il bromo elementale in presenza di carbone ad un temperatura di 300 °C:
B2O3 + 3 C + 3 Br2 → 2 BBr3 + 3 CO.
Segue distillazione sotto vuoto.
In alternativa può essere preparato dagli elementi, a temperature inferiori senza produrre CO come sottoprodotto.
2 B + 3 Br2 → 2 BBr3
La tipica preparazione da laboratorio, ove non si ha disponibilità di tale reagente, prevede la reazione del boro trifluoruro, puro, con alluminio tribromuro (analogamente si può ottenere il tricloruro usando alluminio tricloruro).
BF3 + AlBr3 → 2 BBr3 + AlF3
Le difficoltà sono diverse: in primis, l'uso di boro trifluoruro anidro. Questo composto, che come il fratello bromuro fuma all'aria, è estremamente corrosivo, libera HF gas e attacca il vetro con estrema facilità, oltre a provocare danni ad oggetti e persone con cui entra in contatto.
Procurarselo e maneggiarlo non è cosa da tutti... Diciamo che sarebbe più facile procurarsi dell'AlBr3  La resa è buona.
Altro metodo alternativo prevede l'uso di KBF4 al posto del BF3 ma le rese sono basse. KBF4 si ottiene per reazione dell'acido borico con HF 40%, cui segue neutralizzazione con KOH usando l'arancio metile come indicatore... Ma non è questo l'argomento.
Chiudo postandovi qualche utilizzo in chimica organica di tale composto.
(A) Scissione di eteri. I reagenti a base di boro sono particolarmente versatili per la scissione di legami C–O, e portano ad un alchile bromuro e ad un alcossiborano che viene poi idrolizzato nel corrispondente alcole.
Gli alchi aril eteri sono scissi sul legame alchile–ossigeno, a dare il corrispondente fenolo e l'alchile bromuro. Comunque, la scissione di dialchil eteri misti di solito avviene al legame carbonio–ossigeno più sostituito, a dare alchil bromuri secondari o terziari.
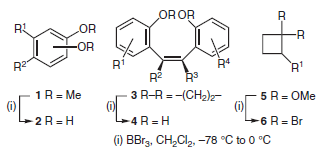
Nella scissione di aril metil eteri, il boro tribromuro è più efficace rispetto ad altri reagenti come lo iodotrimetilsilano. Quando diversi gruppi alcossi sono presenti sull'anello aromatico (1), il trattamento con BBr3 porta alla deprotezione di tutti quanti con rese elevate (2).
Mayekar et al. hanno rimosso il gruppo spacer dimetilene da stilbeni ciclici 3 ottenendo lo stilbene isomero aciclico geometricamente puro 4 con buona resa, senza isomerizzazione del doppio legame dello stilbene.
Recentemente, Nordvik e Brinker hanno descritto una nuova via di sintesi di dibromociclobutani geminali 6 che coinvolge il trattamento del corrispondente ciclobutanone acetale 5 con BBr3.
La resa è buona.
Altro metodo alternativo prevede l'uso di KBF4 al posto del BF3 ma le rese sono basse. KBF4 si ottiene per reazione dell'acido borico con HF 40%, cui segue neutralizzazione con KOH usando l'arancio metile come indicatore... Ma non è questo l'argomento.
Chiudo postandovi qualche utilizzo in chimica organica di tale composto.
(A) Scissione di eteri. I reagenti a base di boro sono particolarmente versatili per la scissione di legami C–O, e portano ad un alchile bromuro e ad un alcossiborano che viene poi idrolizzato nel corrispondente alcole.
Gli alchi aril eteri sono scissi sul legame alchile–ossigeno, a dare il corrispondente fenolo e l'alchile bromuro. Comunque, la scissione di dialchil eteri misti di solito avviene al legame carbonio–ossigeno più sostituito, a dare alchil bromuri secondari o terziari.
Nella scissione di aril metil eteri, il boro tribromuro è più efficace rispetto ad altri reagenti come lo iodotrimetilsilano. Quando diversi gruppi alcossi sono presenti sull'anello aromatico (1), il trattamento con BBr3 porta alla deprotezione di tutti quanti con rese elevate (2).
Mayekar et al. hanno rimosso il gruppo spacer dimetilene da stilbeni ciclici 3 ottenendo lo stilbene isomero aciclico geometricamente puro 4 con buona resa, senza isomerizzazione del doppio legame dello stilbene.
Recentemente, Nordvik e Brinker hanno descritto una nuova via di sintesi di dibromociclobutani geminali 6 che coinvolge il trattamento del corrispondente ciclobutanone acetale 5 con BBr3.
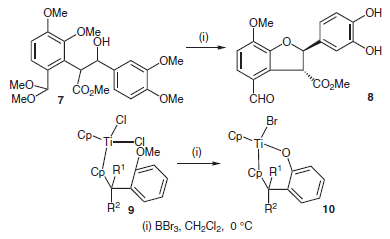
 (B) Scissione di eteri e ciclizzazione. Queste trasformazioni tandem comportando la deprotezione di un etere e la conseguente ciclizzazione intramolecolare. Questa strategia è stata usata per la ciclizzazione totalmente diastereoselettiva di diverse molecole precursori come 7, ottenuta attraverso un reazione tipo-aldolica, a dare una erie di arilidrobenzofurani idrossilati 8, che sono spesso strutture chiave in prodotti naturali. Qian et al. hanno studiato la ciclizzazione intramolecolare di complessi ciclopentadienil titanio 9 a formare complessi titanossaciclo 10 promossa da BBr3. È stato proposto un probabile meccanismo a due passaggi che coinvolge uno scambio di alogeno ed una eliminazione intramolecolare.
(B) Scissione di eteri e ciclizzazione. Queste trasformazioni tandem comportando la deprotezione di un etere e la conseguente ciclizzazione intramolecolare. Questa strategia è stata usata per la ciclizzazione totalmente diastereoselettiva di diverse molecole precursori come 7, ottenuta attraverso un reazione tipo-aldolica, a dare una erie di arilidrobenzofurani idrossilati 8, che sono spesso strutture chiave in prodotti naturali. Qian et al. hanno studiato la ciclizzazione intramolecolare di complessi ciclopentadienil titanio 9 a formare complessi titanossaciclo 10 promossa da BBr3. È stato proposto un probabile meccanismo a due passaggi che coinvolge uno scambio di alogeno ed una eliminazione intramolecolare.
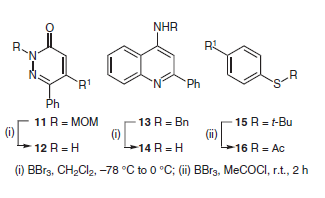
 (C) Scissione di amine e tioli. Dato che BBr3 può anche scindere i legami C–N e C–S in condizioni di reazione blande, è stato usato per la rimossione di gruppi protettivi amine e tioli.
Sotelo et al. hanno presentato una procedura selettiva per la scissione di un gruppo metossimetile in posizione 2 di piridazinoni acido-labili
11 senza intaccare i doppi legami della molecola. Paliakov e Strekowski hanno riportato il trattamento di benzilamino chinoline 13 con BBr3 a dare i corrispondenti amino derivati 14 con rese ottime, usando corti tempi di reazione. Recentemente, la terminazione tert-butile, un gruppo protettivo per tioli resistente a basi, è stata sostituita facilmente da un labile terminazione acetile in una reazione one pot (15 → 16), usando una miscela di BBr3 e acetile cloruro. Questa strategia è stata usata nella sintesi di oligo(fenilenevinileni) (OPVs),
nuovi materiali organici con proprietà elettriche ed ottiche.
(C) Scissione di amine e tioli. Dato che BBr3 può anche scindere i legami C–N e C–S in condizioni di reazione blande, è stato usato per la rimossione di gruppi protettivi amine e tioli.
Sotelo et al. hanno presentato una procedura selettiva per la scissione di un gruppo metossimetile in posizione 2 di piridazinoni acido-labili
11 senza intaccare i doppi legami della molecola. Paliakov e Strekowski hanno riportato il trattamento di benzilamino chinoline 13 con BBr3 a dare i corrispondenti amino derivati 14 con rese ottime, usando corti tempi di reazione. Recentemente, la terminazione tert-butile, un gruppo protettivo per tioli resistente a basi, è stata sostituita facilmente da un labile terminazione acetile in una reazione one pot (15 → 16), usando una miscela di BBr3 e acetile cloruro. Questa strategia è stata usata nella sintesi di oligo(fenilenevinileni) (OPVs),
nuovi materiali organici con proprietà elettriche ed ottiche.
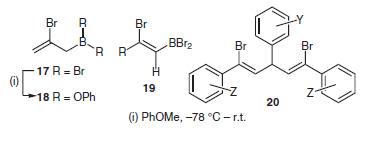
 (D) Addizione ad alleni ed alchini. BBr3 reagisce facilmente con alleni ed alchini a dare prodotti di bromoborazione. Quindi, la reazione di BBr3 con l'allene a –20 °C dà il (2-bromoallil)dibromoborano 17, che può reagire con l'anisolo a dare il (2-bromoallil)difenossiborano 18. Le reazioni di BBr3 con alchini di solito avvengono in modo stereo-, regio-, e chemoselettivo attraverso la syn addizione della terminazione B–Br al legame C≡C, generando il corrispondente (Z)-(2-bromo-1-alchenil)dibromoborano 19. Questi vinilborani sono intermedi versatili che possono essere usati in trasformazioni quali le addizioni a composti carbonilici. Un esempio recente è la reazione di aril aldeidi con due equivalenti di arilacetileni in presenza di BBr3; questa ha generato l'isomero puro (Z,Z)-1,3,5-triaril-
1,5-dibromo-1,4-pentadiene 20.
(D) Addizione ad alleni ed alchini. BBr3 reagisce facilmente con alleni ed alchini a dare prodotti di bromoborazione. Quindi, la reazione di BBr3 con l'allene a –20 °C dà il (2-bromoallil)dibromoborano 17, che può reagire con l'anisolo a dare il (2-bromoallil)difenossiborano 18. Le reazioni di BBr3 con alchini di solito avvengono in modo stereo-, regio-, e chemoselettivo attraverso la syn addizione della terminazione B–Br al legame C≡C, generando il corrispondente (Z)-(2-bromo-1-alchenil)dibromoborano 19. Questi vinilborani sono intermedi versatili che possono essere usati in trasformazioni quali le addizioni a composti carbonilici. Un esempio recente è la reazione di aril aldeidi con due equivalenti di arilacetileni in presenza di BBr3; questa ha generato l'isomero puro (Z,Z)-1,3,5-triaril-
1,5-dibromo-1,4-pentadiene 20.
 (E) Reagenti chirali di boro. L'uso di acidi di Lewis chirali quali catalizzatori per reazioni di Diels–Alder asimmetriche ha trasformato la classica cicloaddizione termica, uno dei processi più versatili ed utili in chimica di sintesi. Complessi ottenuti a partire da pirrolidine chirali e BBr3 sono efficaci catalizzatori per queste cicloaddizioni.
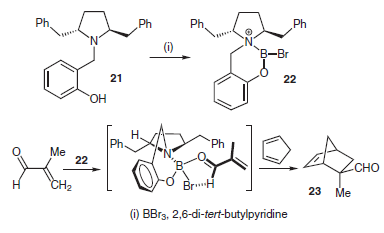
Sprott e Corey recentemente hanno descritto che il trattamento della 2,5-dibenzilpirrolidina 21 con 2,6-di-tert-butilpiridina e BBr3 porta alla formazione di 22, che catalizza la reazione di Diels–Alder del ciclopentadiene e della 2-metacroleina a formare l'addotto eso 23 con una resa del 96% ed un ee del 96%.
(E) Reagenti chirali di boro. L'uso di acidi di Lewis chirali quali catalizzatori per reazioni di Diels–Alder asimmetriche ha trasformato la classica cicloaddizione termica, uno dei processi più versatili ed utili in chimica di sintesi. Complessi ottenuti a partire da pirrolidine chirali e BBr3 sono efficaci catalizzatori per queste cicloaddizioni.
Sprott e Corey recentemente hanno descritto che il trattamento della 2,5-dibenzilpirrolidina 21 con 2,6-di-tert-butilpiridina e BBr3 porta alla formazione di 22, che catalizza la reazione di Diels–Alder del ciclopentadiene e della 2-metacroleina a formare l'addotto eso 23 con una resa del 96% ed un ee del 96%.
I seguenti utenti ringraziano quimico per questo messaggio: rock.angel, Rusty, marco the chemistry, Mario