ale93
2011-04-21 18:28
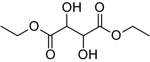
Questo estere etilico è un po' complicato da raggiungere, per via della sua difficoltosa separazione, dato che è molto solubile sia in acqua che in etanolo.
Fortunatamente ha un p.e. abbastanza alto, e questo lo rende separabile per eliminazione dell'EtOH in eccesso.
REAGENTI E ATTREZZATURE NECESSARIE:
-Etanolo 95° non denaturato :infiammabile:
-Acido tartarico :irritante:
-Acido solforico :corrosivo:
-Allhin o altro refrigerante per ricadere
-Apparecchiatura per filtrazione sotto vuoto
PROCEDIMENTO:
Si mescolano 40ml di etanolo 95° con 4ml di acido solforico concentrato, in un pallone a due colli da 100ml.
Si attacca l'allhin e si aggiungono 20g di acido tartarico.
Si scalda il tutto a forte riflusso; dapprima l'acido tartarico si solubilizza, dopo la soluzione intorbidisce. Occorre prolungare il riflusso fino a quando la soluzione torna limpida, occorrono circa 2 ore.
Terminato il riflusso si aggiunge carbonato di sodio a piccole porzioni(non aggiungere acqua) fino a quando cessa l'effervescenza.
A questo punto occorre filtrare la soluzione sotto vuoto, per via dell'elevata viscosità, che renderebbe molto difficile la filtrazione per gravità, si continua a filtrare fino ad ottenere una soluzione perfettamente limpida.
(in questo passaggio purtroppo c'è stata una piccola perdita per una cosa stupida  )
)
A questo punto occorre separare l'estere dall'etanolo, sfruttando il suo elevato punto di ebollizione.
Si scalda la soluzione( dovrebbero essere 40ml, ma come detto prima io ne ho persi 10  ) fino al punto di ebollizione dell'etanolo, e si tiene la temperatura costante fino a quando non si avverte più l'odore di EtOH.
) fino al punto di ebollizione dell'etanolo, e si tiene la temperatura costante fino a quando non si avverte più l'odore di EtOH.
La resa è stata di 6ml (26% della teorica), ma sono comunque soddisfatto dato che non ho previsto futuri utilizzi per questo estere.
Si presenta come un liquido incolore, molto viscoso, d=1,2 p.e.=280°C, dal lieve odore di vino rosso.




 Come fa a decomporre il tartarico a meno di 100°C?
Come fa a decomporre il tartarico a meno di 100°C?
 non lo so...
non lo so...
 Non ho lastrine per TLC, comunque dato che ho messo carbonato di sodio in eccesso e il tartrato di sodio è insolubile in alcool e nell'estere, nono dovrebbe essercene di residuo, ora provo a far evaporare una goccia del prodotto finale e vedo che rimane.
Non ho lastrine per TLC, comunque dato che ho messo carbonato di sodio in eccesso e il tartrato di sodio è insolubile in alcool e nell'estere, nono dovrebbe essercene di residuo, ora provo a far evaporare una goccia del prodotto finale e vedo che rimane.