valeg96
2018-08-02 15:47
Premessa: Questa sintesi prevede la produzione, gestione e smaltimento di cloro gassoso e dei reagenti utilizzati per produrlo, e comporta quindi tutti i rischi legati alla loro gestione. Questa sintesi prevede la produzione di una sostanza (ammonio dicloroioduro) estremamente corrosiva verso i metalli, ossidante e che rilascia iodio e ICl spontaneamente e se mal conservata. Nonostante l’ammonio dicloroioduro sia uno dei peralogenuri più stabili, questa sintesi comporta inevitabili e spesso irrimediabili danni a tutta la strumentazione utilizzata che non sia di vetro: qualsiasi oggetto metallico si corroderà all’istante e qualsiasi oggetto di plastica diventerà viola, adsorbendo iodio. Nel caso del silicone, è reversibile, per le altre plastiche, no. Per questi, ed altri motivi, sconsiglio di riprodurre la metodica esposta.
Il mondo dei composti interalogenici e dei loro derivati è molto ampio, ma possiamo provare a riassumerlo superficialmente in alcune nozioni.
Un ALOGENO è un elemento appartenente al gruppo 17 della tavola periodica (F, Cl, Br, I, At). Quando due alogeni diversi si combinano, in modo quasi sempre diretto, otteniamo una specie molto reattiva e volatile, con grandi capacità alogenanti, chiamata INTERALOGENO: un interalogeno è una specie neutra composta solamente da alogeni, di formula XYn, dove X e Y sono due alogeni diversi ed n = 1, 3, 5, 7. (Es.: ClF, ICl3, BrF5, IF7). Quando un interalogeno idrolizza, origina uno IONE POLIALOGENICO, uno ione poliatomico contenente almeno due alogeni. Uno ione polialogenico può essere un catione o un anione, e può essere ISOPOLIALOGENICO, se contiene alogeni uguali (Es.: [Cl3]+, [I3]-) o ETEROPOLIALOGENICO, se contiene alogeni diversi (Es.: [ICl2]-, [ClF2]-).
Più tradizionalmente, una specie contenente un elevato numero di alogeni (> 2) è chiamato per brevità PERALOGENO/PERALOGENURO. Un peralogenuro può essere ulteriormente definito DIALOGENURO, TRIALOGENURO e così via. Viene da sé che un composto polialogenico e un interalogeno sono delle specie peralogeniche.
L’utilità delle specie peralogeniche viene principalmente dalle loro marcatissime proprietà alogenanti: essendo gli atomi di alogeno tutte specie elettronegative, i peralogenuri sono instabili e forti ossidanti. Ad esempio, un peralogenuro stabile con il quale ho avuto occasione di lavorare è il dicloroiodobenzene, o iodobenzene dicloruro, PhICl2, che si può preparare gorgogliando Cl2 gassoso in iodobenzene in sospensione in cloroformio. Questo agente clorurante è anche un buon ossidante, in quanto fonte di radicali Cl·.
Uno dei peralogenuri più economici da preparare è l’ammonio dicloroioduro, NH4ICl2. È il sale di ammonio dello ione dicloroioduro:
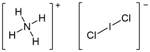
- Reazione diretta tra Cl2 gorgogliato in I2 sospeso in NH4Cl: NH4Cl + Cl2 + ½ I2 ⇌ NH4ICl2
- Reazione “quasi-diretta” tra Cl2 gorgogliato in NH4I:
NH4I + Cl2 ⇌ NH4ICl2
- Durante queste due metodiche, se si addiziona cloro fino a saturazione, si ottiene l’ammonio tetracloroioduro, secondo il seguente equilibrio: NH4ICl2 (rosso scarlatto) + Cl2 ⇌ NH4ICl4 (giallo oro)
La sintesi si basa su un articolo del 1915 di Frederick Daniel Chattaway intitolato “Ammonium Perhaloids”, che riassume le sintesi di quattro peralogenuri di ammonio. La procedura è inoltre presente sul New Dictionary of Chemistry di Stephen Miall, del 1940. Le figure e gli schemi presentati non sono assolutamente categorici, ma devono essere adattati a ciò che si possiede e alla scala prescelta, e ove possibile, migliorati per rendere la sintesi più sicura. Nella sintesi sono coinvolti i seguenti reagenti: Iodio elementare
![[Irritante]](images/irritante.png.pagespeed.ce.KZwWJmvAGL.png)
![[Corrosivo]](images/corrosivo.png.pagespeed.ce.CTVEf8LXM3.png) Ammonio cloruro
Cloro gassoso
Ammonio cloruro
Cloro gassoso ![[Tossico]](images/tossico.png.pagespeed.ce.BU9Uoks0SY.png)
![[Corrosivo]](images/corrosivo.png.pagespeed.ce.CTVEf8LXM3.png)
![[Ossidante]](images/ossidante.png) , prodotto gocciolando acido cloridrico al 15%
, prodotto gocciolando acido cloridrico al 15% ![[Corrosivo]](images/corrosivo.png.pagespeed.ce.CTVEf8LXM3.png) su uno dei seguenti: sodio dicloroisocianurato (NaDCC), acido dicloroioscianurico (DCCA), acido tricloroisocianurico (TCCA), tutti e tre
su uno dei seguenti: sodio dicloroisocianurato (NaDCC), acido dicloroioscianurico (DCCA), acido tricloroisocianurico (TCCA), tutti e tre ![[Ossidante]](images/ossidante.png)
![[Corrosivo]](images/corrosivo.png.pagespeed.ce.CTVEf8LXM3.png) .
Idrossido di sodio in perle, anche impuro, per lo scrubbing dei gas
.
Idrossido di sodio in perle, anche impuro, per lo scrubbing dei gas ![[Corrosivo]](images/corrosivo.png.pagespeed.ce.CTVEf8LXM3.png) .
In un apparato come in figura 1, si prepara una sospensione, in non più di 5-10 mL di acqua distillata (ndr: l'articolo originale dice di usare una "quantità di acqua uguale al cloruro di ammonio", quindi è meglio tenersi sui 5 mL), di 5 g di cloruro di ammonio e di 12-13g g di iodio elementare (reagente in leggero eccesso). Facendo gocciolare HCl al 15% su NaDCC, DCCA o TCCA, si produce un lento e costante flusso di cloro, che viene preventivamente regolato in una beuta o provetta di scrubbing a) con acqua e NaOH al fine di ottenere circa una bolla al secondo. E' utile avere anche una provetta o beuta piena di NaOH solida in perle c) dove inserire il gorgogliatore quando non utilizzato, per evitare fenomeni di risucchio che potrebbero avvenire con la soluzione di NaOH. Il cloro è quindi gorgogliato nella sospensione sotto agitazione b) fino alla dissoluzione di tutti i solidi. Il primo solido a sparire sarà il cloruro di ammonio, seguito dallo iodio. Il gorgogliamento, che provoca un riscaldamento della soluzione, viene interrotto non appena il colore viola/bruno dello iodio libero scompare, e la soluzione appare rosso scarlatto/carminio e limpida.
.
In un apparato come in figura 1, si prepara una sospensione, in non più di 5-10 mL di acqua distillata (ndr: l'articolo originale dice di usare una "quantità di acqua uguale al cloruro di ammonio", quindi è meglio tenersi sui 5 mL), di 5 g di cloruro di ammonio e di 12-13g g di iodio elementare (reagente in leggero eccesso). Facendo gocciolare HCl al 15% su NaDCC, DCCA o TCCA, si produce un lento e costante flusso di cloro, che viene preventivamente regolato in una beuta o provetta di scrubbing a) con acqua e NaOH al fine di ottenere circa una bolla al secondo. E' utile avere anche una provetta o beuta piena di NaOH solida in perle c) dove inserire il gorgogliatore quando non utilizzato, per evitare fenomeni di risucchio che potrebbero avvenire con la soluzione di NaOH. Il cloro è quindi gorgogliato nella sospensione sotto agitazione b) fino alla dissoluzione di tutti i solidi. Il primo solido a sparire sarà il cloruro di ammonio, seguito dallo iodio. Il gorgogliamento, che provoca un riscaldamento della soluzione, viene interrotto non appena il colore viola/bruno dello iodio libero scompare, e la soluzione appare rosso scarlatto/carminio e limpida.









![[Tossico]](images/tossico.png.pagespeed.ce.BU9Uoks0SY.png)
![[Corrosivo]](images/corrosivo.png.pagespeed.ce.CTVEf8LXM3.png)
![[Ossidante]](images/ossidante.png) .
.

I seguenti utenti ringraziano valeg96 per questo messaggio: ohilà, fosgene, Roberto, Copper-65, AminewWar, TrevizeGolanCz, EdoB, NaClO, ClaudioG., Mr.Hyde, ale93