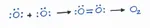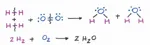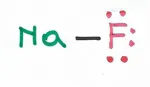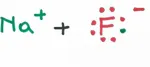longosamuel
2017-09-17 14:05
Buongiorno a tutti.
Premetto che sono una matricola e che di chimica praticamente non ne ho vista nella mia vita.
Mi sto mettendo un po' avanti perchè le lezioni non sono ancora cominciate e mi sono imbattuto nei legami.
Avrei qualche dubbio:
1) L'ossigeno in natura si trova in forma molecolare. Ma un atomo di ossigeno ha due elettroni spaiati; al momento che due atomi di ossigeno mettono in comune due elettroni, rimangono comunque altri due elettroni spaiati: si forma un legame [img=9x11]https://wikimedia.org/api/rest_v1/media/math/render/svg/9be4ba0bb8df3af72e90a0535fabcc17431e540a[/img] tra i due elettroni spaiati?
Inoltre, sempre l'ossigeno molecolare, come fa a legarsi agli atomi di idrogeno per formare l'acqua? Cioè, i due atomi di ossigeno sono già legati tra di loro, ed hanno entrambi messo in comune almeno un elettrone ciascuno. Quindi, ammettendo che non si formi nessun legame pi greco o di altro tipo tra i due elettroni rimanenti, ogni atomo di ossigeno sarebbe in grado di legarsi ad un solo atomo di idrogeno. Come fa quindi a crearsi una molecola d'acqua? Si rompe il legame tra gli atomi di ossigeno? (qualora si formi un legame anche tra i due elettroni rimanenti, ogni atomo di ossigeno rimarrebbe a corto di elettroni spaiati, quindi la possibilità di formare una molecola d'acqua senza slegarsi dall'altro atomo di ossigeno mi sembra ancora più remota)
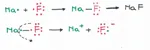
2) Quando si forma un legame ionico: Na+F; perchè non si instaura un legame covalente, ma proprio ionico? Cioè perchè il Fluoro "ruba" (più precisamente accetta) l'elettrone del Sodio piuttosto che metterne in comune uno insieme al Sodio? Io ho provato a rispondere: ho supposto che la differenza di potenziale di ionizzazione sia talmente alta che piuttosto che condividere, gli elementi siano indotti a cedere e accettare. (Anche in ragione della regola dell'ottetto, infatti il Sodio non va verso la stabilità acquisendo un elettrone messo in comune con il Fluoro, mentre diventa stabile cedendone direttamente uno). Il mio dubbio era se il mio ragionamento fosse sensato e se non mi sfuggisse qualcosa.
3) Cosa induce due atomi ad instaurare un legame covalente? Cioè, so che Lewis aveva intuito che due atomi mettessero in comune una coppia di elettroni, ma c'è una spiegazione scientifica non sperimentale? C'è una formula che lo afferma?
Chiedo scusa per la mole di domande, ma sono dubbi piuttosto pressanti per me 
Grazie,
Samuel