al-ham-bic
2011-10-18 20:32
Si parla in questo periodo di riduzioni organiche: eccone una a fagiolo, così uniamo la teoria alla pratica.
In ambiente acido e fortemente riducente, i nitrocomposti aromatici portano alla formazione della corrispondente ammina; è noto per esempio che il classico metodo di produzione dell'anilina parte dal nitrobenzene che viene ridotto con ferro e acido cloridrico diluito.
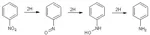
Il processo di riduzione risente fortemente delle condizioni e del pH dell'ambiente, tanto che usando ambienti riducenti intermedi si possono isolare prodotti diversi; per esempio dal nitrobenzene la reazione procede al nitrosobenzene, alla fenilidrossilammina e infine all'anilina.
In ambiente alcalino la situazione è ancora più variegata.
Ho provato una procedura per la sintesi della fenilidrossilammina (quasi identica a quella del Vogel) ed ecco i risultati.
Materiale occorrente
- nitrobenzene C6H5-NO2
- ammonio cloruro NH4Cl
- zinco polvere Zn
- cloruro di sodio
Ricordo che il nitrobenzene va trattato con le necessarie cautele, essendo particolarmente tossico; idem per tutta questa sintesi, che va fatta senza "smanazzare" alcunchè. :tossico:
- In un becker da 250 ml, sciogliere 6 g di NH4Cl in 250 ml di acqua e aggiungere 12 g (10 ml) di nitrobenzene.
Porre su agitatore magnetico e aggiungere in quattro porzioni distanziate di un quarto d'ora un totale di 18 g di zinco in polvere. La reazione Zn/NH4Cl è esotermica e la temperatura si innalza verso i 50° e in una mezz'oretta complessiva il processo di riduzione dovrebbe completarsi e l'odore forte e caratteristico del nitrobenzene dovrebbe sparire. Nel mio caso, avendo usato della polvere di zinco molto vecchia, la temperatura stentava a salire ed ho lasciato in agitazione per un paio di ore, senza riuscire ad eliminare del tutto l'odore di mandorle amare.
Sicuramente la riduzione non è stata completa, ma essendo questa una sintesi "provvisoria" (ved. in seguito) mi sono accontentato della situazione non essendo questa volta importante la questione della resa.
Filtrare ora alla pompa l'abbondante residuo di zinco e suoi ossidi derivati dalla reazione; il filtrato è un liquido giallastro un po' torbido.
La fenilidrossilammina si separa da questo liquido saturandolo con NaCl (ne servono 35 g ogni 100 ml) inizialmente sotto forma di un precipitato flocculento molto voluminoso di colore giallastro.
Filtrare su buchner, ridisciogliere nella minima quantità di acqua calda (solub. 1/20), raffreddare in ghiaccio e e riprecipitare ancora saturando con NaCl.
Per separarla completamente dal cloruro di sodio residuo sciogliere in etere, decantare ed evaporare.
Ho ottenuto 5 g di prodotto (47%), in aghetti giallastri marroncini che rapidamente scuriscono all'aria, come si può vedere in foto.
La fenilidrossilammina è estremamente reattiva e si può conservare per un po' di tempo solo se molto pura, quindi sarebbe comunque destinata ad una sorte "provvisoria" e l'ho fatta solo per testare la procedura di sintesi, che funziona.
L'impiego sicuramente più interessante che se ne potrebbe fare è la sintesi del Cupferron, partendo dalla fen.idr.amm. appena prodotta.
Il cupferron è un bellissimo reattivo per il rame e per il ferro ed è il sale di ammonio della N-nitrosofenilidrossilammina.
(E' una nitrosoammina :tossico: :tossico: !).
La sua sintesi presuppone però l'impiego di grandi quantità di ammoniaca gassosa proveniente da bombola e quindi tale lavoro è del tutto improponibile per un home-lab.
Considerazioni: già il giorno seguente la sintesi, il prodotto, tenuto volutamente all'aria, era diventato schifosamente scuro.
Dopo una settimana si era tramutato in un liquido quasi nero. Dopo un mese si era solidificato in una massa vagamente cristallino-fibrosa, di colore molto scuro ed ora è stabile così.
Mi piacerebbe assai conoscere l'ignota composizione di queste trasformazioni, che non ho trovato in letteratura.
I seguenti utenti ringraziano al-ham-bic per questo messaggio: arkypita, **R@dIo@TtIvO**

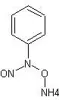
 Saranno forse coinvolti SET, reazioni radicaliche... chi più ne ha più ne metta
Saranno forse coinvolti SET, reazioni radicaliche... chi più ne ha più ne metta  Certo è che la cascata riduttiva che dal nitro va all'amino è qualcosa di molto interessante.
Nel gruppo di ricerca in cui lavoravo sintetizzavamo nitroso arili per poi accoppiarli
Certo è che la cascata riduttiva che dal nitro va all'amino è qualcosa di molto interessante.
Nel gruppo di ricerca in cui lavoravo sintetizzavamo nitroso arili per poi accoppiarli  con alchini terminali più o meno complessi al fine di ottenere indoli e/o N-idrossi-indoli... e mi sono fatto una bella cultura in merito a queste riduzioni. Ci sarebbe da parlare per ore se non giorni.
Tipicamente la riduzione da nitro a nitroso si può fare o con complessi carbonilici di Rh e Ru in cui il complesso viene stabilizzato da altri ligandi quali ad esempio il ciclopentadienile... ma noi preferivamo usare sodio tungstato in presenza di acido ortofosforico... il prodotto si isolava tramite colonna cromatografica flash, anche se spesso era sporco di diazobenzene... le rese non sono sempre delle migliori ma quello che separavamo era abbastanza per le nostre mini reazioni. La colonna poi era affascinante: non perché amassimo farla ma perché il nitroso composto cromaticamente si seperava bene dal diazobenzene... era d'aiuto
con alchini terminali più o meno complessi al fine di ottenere indoli e/o N-idrossi-indoli... e mi sono fatto una bella cultura in merito a queste riduzioni. Ci sarebbe da parlare per ore se non giorni.
Tipicamente la riduzione da nitro a nitroso si può fare o con complessi carbonilici di Rh e Ru in cui il complesso viene stabilizzato da altri ligandi quali ad esempio il ciclopentadienile... ma noi preferivamo usare sodio tungstato in presenza di acido ortofosforico... il prodotto si isolava tramite colonna cromatografica flash, anche se spesso era sporco di diazobenzene... le rese non sono sempre delle migliori ma quello che separavamo era abbastanza per le nostre mini reazioni. La colonna poi era affascinante: non perché amassimo farla ma perché il nitroso composto cromaticamente si seperava bene dal diazobenzene... era d'aiuto  (Ho un po' esagerato
(Ho un po' esagerato 
 ma è una autolesionista di natura!
ma è una autolesionista di natura! 