quimico
2011-11-20 17:56
Nel 2004 sul J. AM. CHEM. SOC. 2004, 126, 12790-12791, Michael T. Crimmins* and Jin She (Department of Chemistry, Venable and Kenan Laboratories of Chemistry, UniVersity of North Carolina at Chapel Hill, Chapel Hill, North Carolina 27599-3290) pubblicarono un interessante articolo, dal titolo Sintesi totale enantioselettiva della (+)-gigantecina: Impiego della reazione glicolato aldolica asimmetrica.
Le piante della famiglia delle Annonaceae producono un abbondante collezione di metaboliti altamente bioattivi con acidi grassi C35-C371. È stato trovato che queste acetogenine portavano ad una potente riduzione dei livelli di ATP tramite l'inibizione del complesso I (NADH, ubichinone ossidoreduttasi)
dei sistemi di trasporto mitocondriale in mammiferi ed insetti e l'inibizione della NADH ossidasi delle membrane plasmatiche delle cellule tumorali2.
Di conseguenza, esse interrompono i meccanismi di resistenza determinati dall'ATP ed hanno mostrato un'attività verso tipi di tumore resistenti a cocktails di farmaci3. Le tre classi principali di acetogenine annonacee sono le sottoclassi dei monotetraidrofurano, dei bis-THF adiacente, e dei bis-THF non adiacenti.
La significativa attività biologica delle acetogenine, così come le loro interessanti e diverse strutture, hanno stimolato un considerevole interesse per quanto concerne la loro sintesi chimica4.
La gigantecina (1), una rappresentativa acetogenina bis-THF non adiacente, fu isolata dalla corteccia del Goniothalamus giganteus nel sud-est asiatico5 e dai semi della pianta brasiliana Annona coriacea6. La configurazioni relativa ed assoluta della gigantecina furono assegnate dopo approfondite analisi spettroscopica e con l'ausilio di agenti derivatizzanti chirali (estere dell'acido di Mosher o acido α-metossi-α-trifluorometilfenilacetico, MTPA), e l'assegnazione venne confermata tramite analisi ai raggi X su cristallo singolo5,6.
La gigantecina ha mostrato una potente citotossicità nei confronti delle linee cellulari tumorali umane A-549 (carcinoma polmoni), HT-29 (adenocarcinoma colon), MCF-7 (adenocarcinoma mammella), e U251MG (glioblastoma multiforme) a ED50 di 0.4, 0.001, 4.3, e 0.003 μg/mL, rispettivamente5.
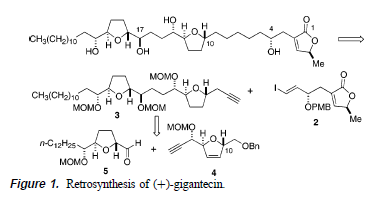 Qui gli autori rendono pubblica la prima sintesi totale della (+)-gigantecina7.
La sintesi sfrutta un protocollo aldolico asimmetrico modificato che usa enolati di clorotitanio di ossazolidinon glicolati. Strategicamente, la gigantecina fu immaginata derivata da un assemblaggio convergente
di tre subunità chiave (Figure 1).
Qui gli autori rendono pubblica la prima sintesi totale della (+)-gigantecina7.
La sintesi sfrutta un protocollo aldolico asimmetrico modificato che usa enolati di clorotitanio di ossazolidinon glicolati. Strategicamente, la gigantecina fu immaginata derivata da un assemblaggio convergente
di tre subunità chiave (Figure 1).
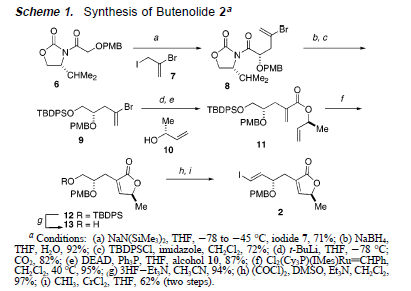 L'alchilazione dell'enolato di sodio dell'ossazolidinon glicolato 6 con lo ioduro allilico 7 è avvenuta con buone rese (71%) e con eccellente diastereoselettività (>98:2)10. L'ausiliario chirale è stato rimosso riduttivamente, e l'alcole primario derivante è stato protetto come TBDPS etere a dare il vinil bromuro 9. Lo scambio litio-alogeno
del bromuro 9 e la reazione con CO2 ha prodotto il derivato acido acrilico, che in modo pulito ha dato l'estere 11 subito dopo inversione dell'alcole 10 nelle condizioni di Mitsunobu11. Il diene 11 è stato trattato con il catalizzatore di Grubbs di seconda generazione12 producendo il butenolide 12 con una resa del 95%. La rimozione del silil etere del 12 ha fornito l'alcole primario 13. L'alcole 13 è stato ossidato ad aldeide, la quale ha subito un'olefinazione di Takai13 a dare il vinil ioduro richiesto 2.
Le sintesi sia dell'alchino 4 C9-C16 che dell'aldeide 5 C17-C34 sono state fondante sull'applicazione di un protocollo sviluppato recentemente per le reazioni aldoliche asimmetriche di complessi enolati di clorotitanio di glicolil ossaziolidinoni14. Il glicolato 15 è stato preparato in tre passaggi semplici dall'(S)-benzil glicidil etere 14 come mostrato nello Schema 2.
L'alchilazione dell'enolato di sodio dell'ossazolidinon glicolato 6 con lo ioduro allilico 7 è avvenuta con buone rese (71%) e con eccellente diastereoselettività (>98:2)10. L'ausiliario chirale è stato rimosso riduttivamente, e l'alcole primario derivante è stato protetto come TBDPS etere a dare il vinil bromuro 9. Lo scambio litio-alogeno
del bromuro 9 e la reazione con CO2 ha prodotto il derivato acido acrilico, che in modo pulito ha dato l'estere 11 subito dopo inversione dell'alcole 10 nelle condizioni di Mitsunobu11. Il diene 11 è stato trattato con il catalizzatore di Grubbs di seconda generazione12 producendo il butenolide 12 con una resa del 95%. La rimozione del silil etere del 12 ha fornito l'alcole primario 13. L'alcole 13 è stato ossidato ad aldeide, la quale ha subito un'olefinazione di Takai13 a dare il vinil ioduro richiesto 2.
Le sintesi sia dell'alchino 4 C9-C16 che dell'aldeide 5 C17-C34 sono state fondante sull'applicazione di un protocollo sviluppato recentemente per le reazioni aldoliche asimmetriche di complessi enolati di clorotitanio di glicolil ossaziolidinoni14. Il glicolato 15 è stato preparato in tre passaggi semplici dall'(S)-benzil glicidil etere 14 come mostrato nello Schema 2.
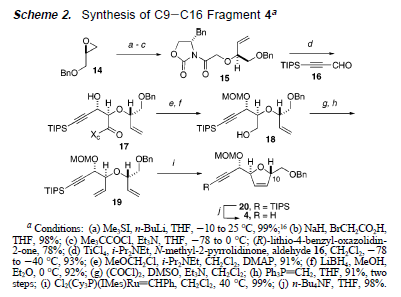 Il glicolato 15 è stato trattato con TiCl4 (1.05 equiv) e i-Pr2NEt (2.5 equiv) per 1 h a -78 °C poi con N-metil-2-pirrolidinone (1.0 equiv) a -78 °C per 10 min.
L'aldeide 16 è stata aggiunta all'enolato poi si è lasciata salire la temperatura a -40 °C. Questa procedura ha portato ad un reazione aldolica altamente diastereoselettivo portando all'alcole 17 con una resa del 93% e ad una dr >20:1 (isomero maggioritario:tutti gli altri isomeri). La protezione dell'alcole secondario come MOM etere e la rimozione riduttiva dell'ausiliario hanno dato l'alcole 18. L'alcole primario 18 è stato ossidato nelle condizioni di Swern15 e l'aldeide è stata immediatamente convertita nell'alchene 19.
Il trattamento del diene 19 con il catalizzatore di Grubbs di seconda generazione12 ha portato alla formazione selettiva del diidrofurano 20 con una resa elevata senza alcune indicazione della reazione dell'acetilene. Il gruppo TIPS terminale è stato prontamente rimosso portando all'alchino voluto 4.
Il glicolato 15 è stato trattato con TiCl4 (1.05 equiv) e i-Pr2NEt (2.5 equiv) per 1 h a -78 °C poi con N-metil-2-pirrolidinone (1.0 equiv) a -78 °C per 10 min.
L'aldeide 16 è stata aggiunta all'enolato poi si è lasciata salire la temperatura a -40 °C. Questa procedura ha portato ad un reazione aldolica altamente diastereoselettivo portando all'alcole 17 con una resa del 93% e ad una dr >20:1 (isomero maggioritario:tutti gli altri isomeri). La protezione dell'alcole secondario come MOM etere e la rimozione riduttiva dell'ausiliario hanno dato l'alcole 18. L'alcole primario 18 è stato ossidato nelle condizioni di Swern15 e l'aldeide è stata immediatamente convertita nell'alchene 19.
Il trattamento del diene 19 con il catalizzatore di Grubbs di seconda generazione12 ha portato alla formazione selettiva del diidrofurano 20 con una resa elevata senza alcune indicazione della reazione dell'acetilene. Il gruppo TIPS terminale è stato prontamente rimosso portando all'alchino voluto 4.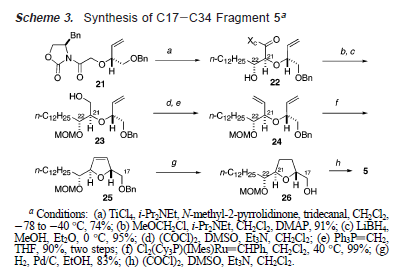 Ancora una volta, è stata usata la reazione aldolica asimmetrica promossa da NMP, in questo caso per creare i centri stereogenici su C21 e C22. L'alcole 22 è stato ottenuto con una resa del 74% (>15:1 dr) dopo esposizione del glicolato 21 (ent-15) alle condizioni dell'aldolica identiche a quelle descritte sopra con l'eccezione dell'uso la tridecanale come componente aldeidica. La protezione dell'alcole secondario come MOM etere seguita da riduzione del carbonile del glicolato ha dato l'alcole 23. L'ossidazione dell'alcole e l'olefinazione dell'aldeide ottenuta ha fornito il diene 24. Il diene 24 è stata sottosposto alla catalisi di Grubbs12 come in precedenza, portando alla formazione del diidrofurano 25. Il trattamento del diidrofurano 25 con idrogeno in presenza di Pd/C ha avuto l'effetto concomitante di ridurre l'alchene ed idrogenolizzare il benzil etere in C17 a dare 26. L'alcole 26 sul C17 è stato quindi convertito all'aldeide 5 nelle condizioni di Swern15.
Con i tre frammenti richiesti in mano, il loro assemblaggio a (+)-gigantecina è stato intrapreso. Il metodo di Carreira per l'addizione dell'acetiluro asimmetrica8 è stato scelto per l'addizione dell'acetilene 4 all'aldeide 5 poichè altri avevano notato bassa diastereoselettività in addizioni simili senza additivi chirali17. Nel caso, l'addizione dell'acetilene 4 a Zn(OTf)2 e (-)-N-metilefedrina in toluene seguita dall'addizione dell'aldeide 5 produceva l'alcole propargilico 27 con una resa del 70% (due passaggi inclusa l'ossidazione di Swern) quale singolo stereoisomero rilevabile (Schema 4).
Ancora una volta, è stata usata la reazione aldolica asimmetrica promossa da NMP, in questo caso per creare i centri stereogenici su C21 e C22. L'alcole 22 è stato ottenuto con una resa del 74% (>15:1 dr) dopo esposizione del glicolato 21 (ent-15) alle condizioni dell'aldolica identiche a quelle descritte sopra con l'eccezione dell'uso la tridecanale come componente aldeidica. La protezione dell'alcole secondario come MOM etere seguita da riduzione del carbonile del glicolato ha dato l'alcole 23. L'ossidazione dell'alcole e l'olefinazione dell'aldeide ottenuta ha fornito il diene 24. Il diene 24 è stata sottosposto alla catalisi di Grubbs12 come in precedenza, portando alla formazione del diidrofurano 25. Il trattamento del diidrofurano 25 con idrogeno in presenza di Pd/C ha avuto l'effetto concomitante di ridurre l'alchene ed idrogenolizzare il benzil etere in C17 a dare 26. L'alcole 26 sul C17 è stato quindi convertito all'aldeide 5 nelle condizioni di Swern15.
Con i tre frammenti richiesti in mano, il loro assemblaggio a (+)-gigantecina è stato intrapreso. Il metodo di Carreira per l'addizione dell'acetiluro asimmetrica8 è stato scelto per l'addizione dell'acetilene 4 all'aldeide 5 poichè altri avevano notato bassa diastereoselettività in addizioni simili senza additivi chirali17. Nel caso, l'addizione dell'acetilene 4 a Zn(OTf)2 e (-)-N-metilefedrina in toluene seguita dall'addizione dell'aldeide 5 produceva l'alcole propargilico 27 con una resa del 70% (due passaggi inclusa l'ossidazione di Swern) quale singolo stereoisomero rilevabile (Schema 4).
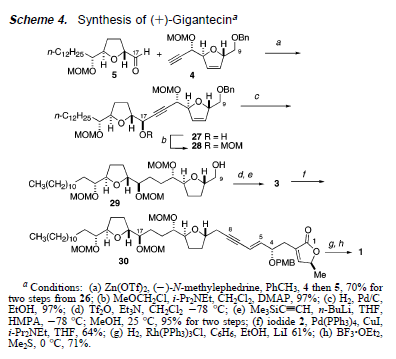 L'idrossile in C17 è stato protetto come MOM etere a dare 28. Il trattamento dell'enino 27 con idrogeno in presenza di Pd/C ha portata alla concomitante riduzione dei doppi e tripli legami così come alla rimozione del benzil etere in C9 a dare l'alcole 29. La formazione del triflato al C9 con la sua conseguente sostituzione tramite litio trimetilsililacetiluro ha fornito l'acetilene 3 con buon rese. Il legame C-C finale è stato modellato tramite coupling mediato da palladio9 dell'acetilene 3 con il vinil ioduro 2 a dare l'enino 30. L'idrogenazione selettiva4d dell'enino C5-C8 seguita da rimozione4d dei gruppi protettivi ha portato al completamento della sintesi della (+)-gigantecina.
La gigantecina sintetica era identica (1H-, 13C-NMR, [α]24D) al materiale naturale.
La prima sintesi totale dell'acetogenina annonacea (+)-gigantecina è stata completata in una maniera enantioselettiva in 19 passaggi lineari dal benzil glicidil etere commercialmente disponibile.
L'idrossile in C17 è stato protetto come MOM etere a dare 28. Il trattamento dell'enino 27 con idrogeno in presenza di Pd/C ha portata alla concomitante riduzione dei doppi e tripli legami così come alla rimozione del benzil etere in C9 a dare l'alcole 29. La formazione del triflato al C9 con la sua conseguente sostituzione tramite litio trimetilsililacetiluro ha fornito l'acetilene 3 con buon rese. Il legame C-C finale è stato modellato tramite coupling mediato da palladio9 dell'acetilene 3 con il vinil ioduro 2 a dare l'enino 30. L'idrogenazione selettiva4d dell'enino C5-C8 seguita da rimozione4d dei gruppi protettivi ha portato al completamento della sintesi della (+)-gigantecina.
La gigantecina sintetica era identica (1H-, 13C-NMR, [α]24D) al materiale naturale.
La prima sintesi totale dell'acetogenina annonacea (+)-gigantecina è stata completata in una maniera enantioselettiva in 19 passaggi lineari dal benzil glicidil etere commercialmente disponibile.