Max Fritz
2011-03-11 09:24
ATTENZIONE:
Il tellurio, come già ribadito, è molto tossico per ingestione e respirazione.
L'idrogeno tellururo, analogamente ai suoi simili come H2Se, AsH3, è letale in quantità molto piccole. Inoltre si decompone in presenza di tracce anche molto piccole di acqua o ossigeno a dare tellurio metallico che quindi può depositarsi sulle mucose dopo l'inalazione!!!!! L'esperimento va eseguito all'aperto, con piccolissime quantità, con tranquillità e prudenza. NON bisogna MAI annusare direttamente i gas emessi: durante la reazione tra Al2Te3 ed acqua l'odore si percepisce anche a distanza, senza dover rischiare una grave intossicazione!!!!
Reagenti:
-Alluminio polvere
-Tellurio pezzi
-Acqua distillata
-Sodio ipoclorito sol. dil.
-Idrogeno perossido 30%
Procedura:
Si miscelano e si omogeneizzano in un mortaio 0,27g di polvere di alluminio e 1,9g di tellurio, nel rapporto stechiometrico 2:3 (guanti e mascherina antipolvere!!!!).
Si pone la miscela in un crogiolo resistente alle elevate temperature e la si innesca con una forte fiamma al butano (indossare occhialini di protezione!!). Allontanarsi immediatamente al momento dell'innesco, anche se la reazione è fulminea e dura veramente poco.
Sul fondo rimarrà una massa molto simile al Te elementare, solo un po' più scura e con qualche riflesso bluastro. Questa viene rotta in pezzetti (indossare guanti e mascherina antipolvere!!)
Alcuni pezzetti vengono posti all'aperto in un becher con circa 20ml di acqua.
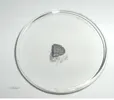
La reazione è abbastanza vivace, accompagnata dallo sfrigolare e dalla continua produzione di gas. L'acqua si colora di nero profondo e torbido, sulla superficie galleggiano bellissime foglie argentate e luminose di tellurio elementare, mentre le pareti stesse del becher si ricoprono di uno strato di Te molto sottile, come uno specchio (nella foto il becher specchiato di tellurio dopo essere stato internamente sciacquato):
Osservazioni:
Senza bisogno di avvicinarsi troppo, a circa un metro di distanza, si sentirà un odore molto caratteristico, simile a mio parere a SiH4, a PH3 e un po' meno a H2Se. L'odore pur essendo lieve è molto penetrante e rimane nelle narici per parecchie ore, dando non poco fastidio. Anche nel caso di quantità minime inalate consiglio sciacqui nasali molto profondi e ripetuti al termine dell'esperimento (non so realmente quanto possano essere utili e d'altronde, non avendo sviluppato alito al tellurio, penso di averne respirata una quantità veramente irrisoria, ma è meglio prevenire!!!). Per quanto riguarda il confronto con H2Se, io trovo il tellururo di idrogeno molto molto molto più penetrante, ma, a livello soggettivo, meno vomitevole. H2Se ha decisamente un odore più organico, a differenza di H2Te che ha per certi versi un odore quasi "metallico". Alcune letterature, come ad esempio il Sidgwick, tuttavia, sostengono che il tellururo di idrogeno sia peggiore del rispettivo con Se. Vi riporto quanto viene detto:
"Hydrogen telluride H2Te is made like the selenide by the action of acids on metallic tellurides, especially that of aluminium Al2Te3, and must be purified by freezing out. Its vapour density is normal. It forms a pale yellow liquid and a colourless solid; it is even more offensive in smell than the selenide, and at least as poisonous. It is the least stable of the four gases, the affinity for hydrogen always falling as the atomic weight increases. It decomposes alone and in the cold unless it is quite dry; like H2Se if it is pure and dry it is not decomposed by light. It is fairly soluble in water, but the solution soon begins to deposit tellurium."
Le due reazioni coinvolte:
2Al + 3 Te ===> Al2Te3
Al2Te3 + 3H2O ===> 3H2Te + Al2O3
Termino con un consiglio pratico: sodio ipoclorito seguito da perossido d'idrogeno concentrato è il miglior metodo che son riuscito ad inventarmi per rimuovere piccoli residui di tellururi: il principio sta nell'ossidare il Te-2 in sostanze più stabili, meno volatili o almeno solubili in acqua. Nella reazione tuttavia si sviluppa anche Cl2
I seguenti utenti ringraziano Max Fritz per questo messaggio: ale93




 perchè a breve farò delle sintresi col tellurio e volevo verificare che le mie idee fossero corrette, solita storia, recupero totale
perchè a breve farò delle sintresi col tellurio e volevo verificare che le mie idee fossero corrette, solita storia, recupero totale  Come non detto...
Come non detto...