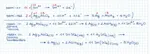Ca0s
2017-02-05 16:07
Dopo aver bilanciato la seguente reazione:
Ag3AsO4(s) + SnSO4(aq) + H2SO4 --> Sn(SO4)2(aq) + AsH3(g) + Ag(s)
Calcolare :
a) il volume minimo di una soluzione di solfato stannoso 0,20 N necessario da aggiungere a 500 mL di acido solforico al 15% in peso (d = 1,10 g/mL) per ridurre completamente 47 g di arseniato d’argento solido;
b) la pressione del gas svolto se, dopo averlo fatto passare su opportuno essiccante, viene raccolto a 20 °C in un recipiente di 4,0 litri;
c) la concentrazione di acido solforico alla fine della reazione (si ritenga costante il volume della soluzione a seguito della reazione).
Svolgimento:
Reaz bilanciata
2AgAsO4 + 5SnSO4 + 5H2SO4 + H+ ----> 5Sn(SO4)2 + 2AsH3 + 6Ag + 8H2O
a)
nAg3AsO4 = 47g/4620524g/mol = 0.1mol
VSnSO4 = ne eq/ 0.2 eq/L = 0.5/0.2 = 2.5L
ne (Ag3AsO4)= n*ze = 0.5 eq
b)
P = nRT/V = 0.6atm
nAsH3= 0.1mol
c)
[H2SO4] = nH2SO4/0.5L = 1.68M
nH2SO4 --> 500mL * 1.1 g/mL = 550g --> 15% --> 82.5g/98.08g/mol = 0.84mol