roberta quattro
2021-06-24 14:23
Buongiorno
In allegato 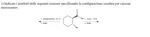
il mio ragionamento è:
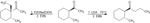
- So che come prima cosa viene strappato un H in alfa al carbonile.
Di H in alfa ne ho due (giusto no?) uno per il CH3 e l'latro che sta sul centro chirale
- in teoria il l'H più acido è quello meno sostituito, quindi quello del metile, però si formerebbe così l'enolo meno sostituito che altro non è l'enolo cinetico. quindi quello che si froma con l'uso di una base molto forte come LDA.
non vado a toccare lo stereocentro
- Caso due dove sono in etanolo, in questo caso si formerà l'enolo termodinamico, più sostituto dove vado a strappare l'H sullo stereocentro. perdo la chiralità.
- l'alchilante potrà legarsi o da davanti o da dietro, essendo che la faccia dietro è già occupata, non gli resta che legarsi davanti
-> qua mi sorge il dubbio, ma se si attacca davanti, allora vuol dire che il gruppo COMe andrà dietro, ma è un gruppo ben più grosso del semplice etile, non è che poi si scambiano e il COMe va davanti per ridurre l'ingombro sterico?
forse sbaglio io e mi faccio troppi problemi dove non esistono
vi ringrazio in anticipo per le risposte
Roberta