ludovicoariosto
2021-07-24 22:25
Salve a tutti,
Nel corso della preparazione ai Giochi della Chimica mi sono imbattuto in un quesito (qui adattato) risalente alla Selezione Nazionale del 2001 che mi è risultato abbastanza ostico (allego foto del quesito e della mia soluzione alla discussione).
Le soluzione corretta risulta essere 109 A. Tuttavia il risultato che io ottengo è 131 A. È la prima volta che provo a risolvere un esercizio del genere e sono insicuro su diversi passaggi. In particolare, dovrei tener conto dei coefficienti stechiometrici della reazione quando calcolo gli equivalenti di cloro gassoso usati nella reazione? Faccio bene ad usare le leggi delle Faraday? E in caso, le sto usando correttamente?
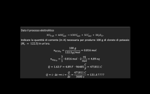
Il mio ragionamento è il seguente: supponendo che vi sia un eccesso di ioni potassio K+, posso calcolare le moli di clorato di potassio a partire dalla sua massa e dalla sua massa molare.
A questo punto, trovo gli equivalenti di cloro gassoso ricorrendo alla stechiometria e alla prima legge di Faraday.
Trovato il numero di equivalenti, conosco quanti Faraday (e quindi quanti Coulomb) attraversano la cella elettrolitica.
Da qui ricorro alla definizione di corrente elettrica per ottenere l'intensità di corrente.
Ringrazio in anticipo chiunque risponderà, anche con una considerazione o un consiglio.