sguonza
2018-06-08 19:49
In un recipiente chiuso alla temperatura T si stabilisce il seguente equilibrio :
X (g) + Y (s) 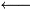 > 2 Z (g) .
> 2 Z (g) .
Noto che la costante Kp = 9 , calcolare la composizione della fase gassosa espressa come % in volume alla pressione di 3 atm.
Ho impostato il problema così: Kp=Kc(P)^delta-n, da cui Kc=9/3^1=3.
E poi sistema con Kc=[Z]^2/[X]=9 e [Z]+[X]=1.
Dal sistema trovo le concentrazioni di X e Z, ma non capisco come passare da queste alla percentuale in volume.
