Geber
2021-02-23 09:38
Visto che stamane ho due minuti liberi, e visto che potrebbe servire ad altri, ho deciso di spendere due parole su questo argomento che spesso viene fatto studiare e chiesto in esami.
Poi mi si è accesa la lampadina dopo la discussione sullo ione solfato  ...
...
Mi scuso se non mi riesce di ordinare le immagini come voglio ma mi si scambiano di continuo.
Premessa:
- Teoria del legame di valenza (VB) considera i legami come combinazioni di orbitali atomici ad un elettrone che si sovrappongono, i quali possono essere o meno ibridizzati. Questo approccio è riscontrabile in molti libri di testo ma è di solito rappresentato usando le convezioni derivate dalla teoria di Lewis, che fu il primo a proporle nell'articolo a firma di G.N. Lewis pubblicato col titolo "The Atom and the Molecule," Journal of the American Chemical Society 38, 762-785 (1916).
- Teoria dell'orbitale molecolare (MO), nella sua forma più semplice (cioè teoria di Hückel e teoria di Hückel estesa), combina orbitali atomici per formare orbitali molecolari in accordo con la simmetria della molecola, riempiendo poi tali orbitali con due elettroni alla volta. Versioni più sofisticate della teoria dell'orbitale molecolare esistono, con diversi modi di considerare le interazioni elettrone-elettrone, queste di solito sono aggiunte al metodo base.
La molecola di monossido di carbonio C≡O, essendo lineare, viene descritta tramite teoria dell'ibridazione come avente atomi ibridizzati sp. L'atomo di carbonio inizia con un elettrone in ognuno dei seguenti orbitai: sp1, sp2, px, py, mostrati schematicamente nella prima figura.
L'atomo di ossigeno iniziare con sei elettroni di valenza, distribuiti (per esempio) così: uno in sp1, due in sp2, due in px, uno in py, come mostrato schematicamente nella seconda figura.
Comunque, gli orbitali ad un elettrone sull'atomo di ossigeno e sull'atomo di carbonio non si accoppiano bene, così possiamo risolvere le cose in uno di due modi:
[list=a]
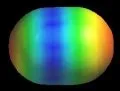
Naturalmente, la teoria del legame di valenza richiede di mischiare questi due modelli (che possono in effetti essere espressi matematicamente); questa è chiamata "risonanza" ed è rappresentata schematicamente nella quinta figura. La vera struttura non è nessuna di questi modelli, ma una combinazione, ed include i contributi derivati dall'elettronegatività che sposta la densità elettronica dall'atomo di carbonio indietro verso l'atomo di ossigeno. La superficie di densità elettronica calcolata (HF/6-31G*) è mostrata nella sesta figura.
Passiamo ora alla teoria MO.
Qualitativamente questa è una rappresentazione estremamente semplice. Gli orbitali atomici di valenza sull'atomo di carbonio e sull'atomo di ossigeno sono, in una prima approssimazione cruda, identici. Dato che il gruppo puntuale molecolare è C∞v, ci sono solo due simmetrie orbitaliche possibili: Σ e Π. Gli orbitali atomici s e pz hanno simmetria Σ, mentre gli orbitali px e py hanno simmetria Π.
Più propriamente parlando, è necessario realizzare che né l'atomo di C né quello di O sono al centro di simmetria della molecola, così che dobbiamo usare combinazioni lineari adattate alla simmetria di orbitali atomici -- che poi si rivelano essere orbitali molecolari. In realtà, di solito non si lavora attraverso l'analisi teorica-di gruppo perché la semplice combinazione visiva ci porta allo stesso posto. E così, al lavoro.
Ci sono due set di orbitali di simmetria Π, ed essi sono mutualmente perpendicolari che non si possano sovrapporre. Essi si combinano per formare due coppie di orbitali molecolari degeneri, una coppia legante (π) e l'altra anti-legante (π*). Questi vengono mostrati nella settima figura.
Ci sono anche due set di orbitali di simmetria Σ, ed essi non sono mutualmente perpendicolari. Possiamo combinarli in due modi equivalenti:
[list=a]
Una volta che abbiamo gli orbitali, tutto ciò che rimane da fare è ordinarli secondo l'energia crescente. Si scopre che l'ordine è come mostrato nella decima figura (ancora, sono i risultati di un calcolo HF/6-31G*), e possiamo riempire gli orbitali molecolari con due elettroni alla volta fino a che si sono usati tutti e dieci gli elettroni di valenza. (Gli orbitali molecolari σ* e π* sono anti-leganti, n è non legante, σ e π sono leganti.)









I seguenti utenti ringraziano Geber per questo messaggio: Mercaptano