Applicazioni sintetiche dell'IBX
Le applicazioni dell'IBX in sintesi organica sono state riassunte in una revisione completa di Pati e co-autori. L'IBX è un ossidante particolarmente utile per l'ossidazione selettiva di alcoli a composti carbonilici, anche in molecole complesse in presenza di altri gruppi funzionali.
Gli alcoli primari sono ossidati dall'IBX in DMSO nelle aldeidi corrispondenti a temperatura ambiente senza sovra-ossidazione ad acidi. Gli alcoli primari chirali sono ossidati senza epimerizzazione, e diversi gruppi funzionali come tioeteri, ammine, acidi carbossilici, esteri, carbossammidi, e sia doppi legami coniugati sia quelli isolati sono compatibili con l'IBX. L'ossidazione selettiva di alcoli usando l'IBX è stata utilizzata in numerose sintesi, quali: la sintesi totale della (+)-wailupemicina B, la sintesi totale della (–)-decarbamoilossisassitossina, la sintesi totale della abissomicina C e della atrop-abissomicina C, la sintesi stereoselettiva della pachastrissamina (jaspine B), le sintesi dei (±)-pterocarpani ed isoflavoni, la sintesi totale della (±)-nitidanina, la sintesi totale della lagunamicina, la sintesi della (–)-agelastatina, le sintesi degli eliannuoli B e D, le sintesi totali delle (–)-subincanadine A e B, la sintesi del metabolita di una spugna marina acido spiculoico A, la sintesi di tetraidroisochinoline estremamente funzionalizzate otticamente pure, e la preparazione di amminoaldeidi protette con lo Fmoc dagli alcoli corrispondenti.
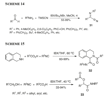
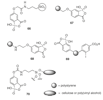
Frigerio e Santagostino riportarono nel 1994 che l'IBX, diversamente dal DMP e da derivati iodossibenzene, ossida senza problemi gli 1,2-dioli ad α-chetoli o α-dichetoni senza scissione del legame C-C del glicole. Più recentemente, Moorthy e colleghi hanno investigato le reazione dell'IBX con diversi dioli vicinali e hanno scoperto che la scissione ossidativa del legame C-C, così come l'ossidazione ad α-chetoli o α-dichetoni, può avvenire in queste reazioni. In soluzioni di DMSO, l'IBX scinde ossidativamente i syn-1,2-dioli tensionati e stericamente ingombrati, mentre i glicoli secondari non ingombrati sono ossidati ad α-chetoli o α-dichetoni. L'utilizzo dell'acido trifluoroacetico come sovente porta ad una efficace frammentazione ossidativa degli 1,2-dioli di tutti i generi. L'ossidazione degli 1,2-dioli usando l'IBX in DMSO è stata utilizzata per la sintesi di α-chetoli, o α-dichetoni. Per esempio, in un passaggio chiave della sintesi totale del metabolite della Streptomyces maritimus wailupemicina B, l'ossidazione con IBX del diolo precursore 13 conduce all'idrossichetone desiderato 14 senza alcuna scissione del legame C-C del glicole (Schema 3).
L'IBX in DMF si è dimostrato essere un reagente eccellente per l'ossidazione di diversi fenoli ad o-chinoni. Questa procedura fu usata per l'ossidazione del fenolo 15 a chinone 16 (Schema 4), un intermedio chiave nella sintesi totale di un nuovo inibitore della cicloossigenasi, il (±)-aifanolo. Pettus e colleghi hanno utilizzato un protocollo simile nella sintesi della (±)-brazilina, un composto tintoriale trovato in estratti alcolici di alberi a cui ci si riferisce collettivamente come legno del Brasile.
La dearomatizzazione ossigenativa mediata da IBX di fenoli che conduce a sintesi cicloesa-2,4- o -2,5-dienonici è un trasformazione sinteticam particolarmente utile. Esempi recenti includono l'uso dell'IBX nei passaggi ossidativi chiave nella sintesi totale dei prodotti naturali polifenolici derivati dal resveratrolo (–)-hopeanolo e (–)-hopeahainolo A, la sintesi dell'acido carnosico e del carnasolo, e la sintesi totale del bissesquiterpene (+)-aquaticolo.
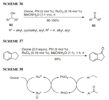
Le applicazioni sintetiche dell'IBX sono notevolmente limitate alla sua insolubilità a temperatura ambiente nella maggior parte dei solventi organici con l'eccezione del DMSO. Comunque, è stata mostrato che l'IBX può essere usato come ossidante efficiente in altri solventi oltre al DMSO a temperature elevate. More e Finney hanno scoperto che gli alcoli primari e secondari possono essere ossidati nei corrispondenti aldeidi o chetoni con rese eccellenti scaldando una miscela dell'alcole e dell'IBX a 55-80 °C nei comuni solventi organici, come cloroformio,
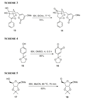
acetone, acetonitrile, etile acetato, e benzene. I sottoprodotti della reazione (principalmente l'acido 2-iodosilbenzoico) possono essere rimossi tramite filtrazione e riossidati a dare circa un 50% di IBX recuperato. Questo metodo fu usato per la preparazione della ribosil aldeide 18 dall'alcole corrispondente 17 (Schema 5), un intermedio chiave nella sintesi stereoselettiva della struttura centrale degli antibiotici poliossina e nikkomicina.
Il valore pratico dell'IBX quale reagente è stato esteso ad una varietà di altre trasformazioni ossidative sinteticamente utili. Nicolaou e colleghi riportarono una procedura one-pot per l'ossidazione di alcoli, chetoni, ed aldeidi alle corrispondenti specie α,β-insature usando l'IBX in condizioni blande. Per esempio, i cicloalcanoli 19 reagiscono con 2 equiv di IBX in una miscela 2:1 o di fluorobenzene/DMSO o di toluene/DMSO sotto blando riscaldamento a dare i corrispondenti chetoni α,β-insaturi 20 con buone rese (Schema 6).
Una simile deidrogenazione ossidativa di un derivato cicloesanonico 21 al corrispondente enone 22 (Schema 7) è stata utilizzata recentemente nella sintesi totale della (–)-anominina.
Kirsch e colleghi hanno ulteriormente investigato le reazioni dell'IBX con i composti carbonilici e scoperto che a seconda del gruppo funzionale in posizione α di un composto carbonilico, la reazione può portare o ad una deidrogenazione ossidativa (cf. Schemi 6 i 7) o ad una α-ossigenazione.
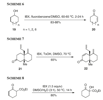
In particolare, i β-cheto esteri e alcuni altri composti carbonilici opportunamente sostituiti possono essere selettivamente α-idrossilati per trattamento con IBX in DMSO acquoso at 50 °C; un esempio rappresentativo della reazione di α-idrossilazione è mostrato nello Schema 8.
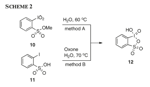
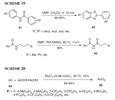
L'IBX è un reagente efficace e selettivo per l'ossidazione di composti aromatici alchil-sostituiti 23 alla posizione benzilica a dare i corrispondenti derivati carbonilici 24 (Schema 9).
Questa reazione è abbastanza generale e può tollerare una varietà di sostituenti sull'anello aromatico. La sovra-ossidazione ai corrispondenti acidi carbossilici non viene osservata anche in presenza di sostituenti elettron-ricchi.
In modo simile all'ossidazione degli alcoli, le ammine secondarie 25 possono essere ossidate con IBX in DMSO fornendo le immine corrispondenti 26 con rese da buone a eccellenti (Schema 10).
Una varietà di eterocicli 28 possono essere sintetizzati per trattamento di aril ammidi, carbammati, e tiocarbammati, ed uree insaturi 27 con IBX (Schema 11). Il meccanismo di questa reazione è stato investigato nel dettaglio. Sulla base degli effetti solventi e di studi con marcatura isotopica con deuterio, fu proposto che la ciclizzazione mediata da IBX di anilidi in THF coinvolgeva un iniziale singolo transfer di elettrone (SET) ad un complesso THF-IBX seguito da deprotonazione, ciclizzazione radicala, e concludeva la terminazione tramite estrazione di idrogeno dal THF.
Una ciclizzazione simile mediata da IBX venne applicata nel protocollo sintetico per la preparazione stereoselettiva di ammino zuccheri.
Studer e Janza riportarono un metodo per la generazione di alcossiammidil radicali a partire dalle corrispondenti alcossiammine acilate usando l'IBX come ossidante SET. Per esempio, la ciclizzazione stereoselettiva 5-eso del rispettivo radicale centrato sull'eteroatomo N porta alla formazione dell'isossazolidina 29 (Schema 12).
L'IBX è stato anche utilizzato per la preparazione delle isossazoline 3,5-disostituite 30. L'ossidazione SET di aldossime sostituite con IBX in diclorometano produce il rispettivo nitrile ossido che quindi subisce addizione 1,3-dipolare con un componente alchenico adatto (Schema 13).
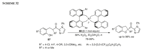
Zhu, Masson, e colleghi hanno riportato una sintesi one-pot, tri-componente degli α-imminonitrili 31 tramite reazione di Strecker ossidativa mediata da IBX/tetrabutilammonio bromuro (Scheme 14). Questa metodologia venne applicata ad una sintesi in due passaggi della indolizidina tramite una cicloaddzione intramolecolare assistita da microonde di una α-imminonitrile.
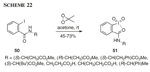
La reazione di Ugi multi-componente ossidativa mediata da IBX della tetraidroisochinolina con isocianuri ed acidi carbossilici conduce a tetraidroisochinoline N- e Cl-funzionalizzate 32 con rese da buone ad eccellenti. Allo stesso modo, la reazione tri-componente di Passerini di un alcole, un acido carbossilico, ed un isonitrile in presenza di IBX conduce alle corrispondenti α-acilossi carbossammidi 33 con rese generalmente alte (Schema 15).
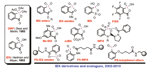
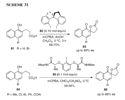
Ulteriori esempi rappresentativi di applicazioni sintetiche dell'IBX includono le seguenti trasformazioni ossidative: l'aromatizzazione di tetraidro-β-carboline in condizioni blande applicata in una sintesi totale dell'alcaloide indolico marino eudistomina U, l'ossidazione di glicosidi nelle corrispondenti 6-carbaldeidi usate come precursori nella sintesi di oligosaccaridi pontati tramite gruppo ammino, l'ossidazione di ammidossime a carbossammidi o nitrili con IBX o IBX/tetraetilammonio bromuro, le idrossilazioni aromatiche di flavonoidi, l'idrossilazione di diacil derivati del resveratrolo, la sintesi della DOPA e di peptidi DOPA tramite ossidazione del residuo tirosina, la preparazione ossidativa di γ-idrossi-α-nitroolefine da α,β-epossichetossime, l'aromatizzazione di 1,4-diidropiridine usando IBX in acqua/acetone in presenza di β-cyclodestrina, la iodoidrossilazione di alcheni e la iodurazione di composti aromatici usando IBX/I2 in acetone acquoso, la conversione di alcheni ed alchini ad α-iodo chetoni usando IBX/I2 in acqua, l'ossidazione di ammine primarie a nitrili, la scissione ossidativa di acetali usando IBX/tetraetilammonio bromuro in acqua, la sintesi one-pot di pirazoli contenenti gruppi trifluorometile tramite reazione tri-componente sequenziale catalizzata da Yb(PFO)3 ed ossidazione mediata da IBX, la tiocianazione ossidativa di indoli, pirroli, ed arilammine, la funzionalizzazione ossidativa degli addotti di Baylis-Hillman, la costruzione di 2-acil furani multi-sostituiti tramite ossidazione/ciclizzazione a cascata mediata da IBX di cis-2-en-4-in-1-oli, la sintesi one-pot di salicilnitrili sostituiti tramite ossidazione delle corrispondenti immine con IBX, la conversione di indoli in isatine usando indio(III) cloruro/IBX, la sintesi di imminochinoni da aniline, e la trasformazione ossidativa di carbossiammidi primarie nei nitrili deomologati di un atomo di carbonio.
In anni recenti, i liquidi ionici hanno guadagnato un riconoscimento come alternative possibili benigne per l'ambiente ai più volatili solventi organici. Diversi gruppi di ricerca hanno studiato i liquidi ionici come mezzi di reazione polari riciclabili per le ossidazioni promesse da IBX. Gli alcoli subiscono blanda ossidazione con IBX nei liquidi ionici [bmim]BF4 e [bmim]PF6 (bmim=1-butil-3-metilimidazolio) a temperatura ambiente in condizioni blande per fornire i corrispondenti composti carbonilici con rese eccellenti con elevata selettività. Risultati simili furono ottenuti per l'ossidazione di alcoli con IBX usando un liquido ionico. Le ossidazioni promosse da IBX sono più veloci nei liquidi ionici quando comparati ai solventi convenzionali come DMSO, DMF, etile acetato, ed acqua. I liquidi ionici recuperati possono essere riciclati in reazioni successive con consistente attività.
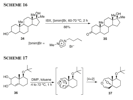
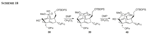
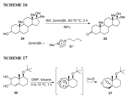
L'IBX immobilizzato nel liquido ionico [bmim]Br fu scoperto essere un reagente efficiente ed ecologico per l'ossidazione del 17α-metilandrostan-3β,17β-diolo 34 a mestanolone 35 con buone rese (Schema 16). Il prodotto è facilmente separato dalla miscela di reazione tramite estrazione con etile etere.