Il nome del topic non ha niente a che veder con il modo bislacco con cui certi esseri giovini scrivono al giorno d'oggi ma è l'esatta pronuncia del cognome del chimico giapponese.
La reazione di Mitsunobu è un metodo versatile e diffusamente usato per il coupling disidratante di un alcole con un acido/pronucleofilo attraverso l'uso di una combinazione di un reagente azo ossidante, più comunemente il dietile azodicarbossilato (DEAD), e di una fosfina che fa da reagente riducente, di solito la trifenilfosfina (TPP), in condizioni di reazione blande e virtualmente neutre.
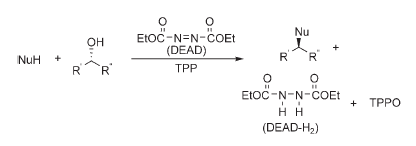
Acidi carbossilici, fenoli, dioli, carboni acidi attivati, immidi, e molto altro possono tutti servire da componente di reazione acido/pronucleofilo.
Perciò, questa reazione può essere usata per preparare esteri, aril eteri, eteri ciclici, legami carbonio–carbonio e carbonio–azoto, e così via.
Oltre al prodotto di coupling desiderato, quali sotto prodotti si ottengono una idrazide quale la dietile idrazinadicarbossilato (DEAD-H2) dal DEAD ed un fosfin ossido quale il trifenilfosfina ossido (TPPO) dalla TPP.
Il Professor Oyo Mitsunobu descrisse per la prima volta la sua reazione eponima nella sua forma più riconoscibile al giorno d'oggi (l'equazione riportata sopra) nel 1967. Comunque, questa nuova reazione fu indubbiamente ispirata dalla precedente osservazione fatta da Mitsunobu stesso, quando era studente del Prof. Teruaki Mukaiyama, e si occupava della sintesi dell'allil fenil etere dalla reazione del fenolo con l'allil dietil fosfito e DEAD, così come trasse ispirazione dalla ricerca di allora del gruppo di Mukaiyama sulle reazioni di condensazione tramite ossidazione-riduzione.
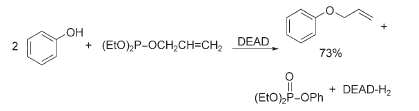
Nella pubblicazione originale, la prima reazione riportata fu quella dell'acido n-valerico con allil dietil fosfito e DEAD per produrre l'allil valerato e il dietil N-(dietil)fosforil idrazodicarbossilato.
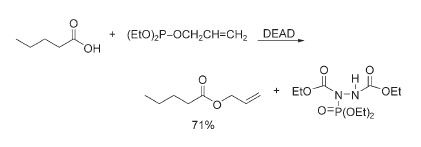
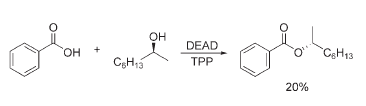
Questa fu seguira dalle reazioni dell'acido benzoico con alcoli in presenza di DEAD e TPP che portarono alla formazione dei corrispondenti esteri con rese eccellenti.
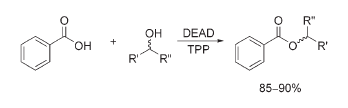
La moderna ubiquità della reazione di Mitsunobu nella chimica di sintesi è dovuta in larga parta dal fatto che il coupling dell'acido/pronucleofilo e dell'alcole normalmente avviene con inversione di configurazione stereochimica del centro del carbinolo. Questo esito stereochimico fu osservato per la prima volta da Mitsunobu ed Eguchi nella reazione del 2-ottanolo arricchito enantiomericamente con l'acido benzoic.
Altri importanti articoli di Mitsunobu riguardanti la reazione che prese il nome da lui includono:
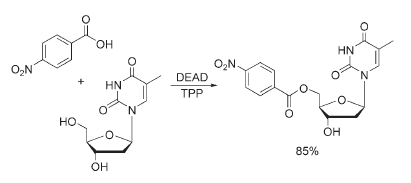
1) l'uso dell'acido 4-nitrobenzoico (4-NBA) per reazioni con alcoli impediti stericamente,
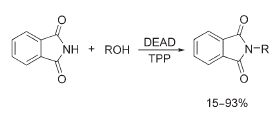
2) l'so della ftalimmide quale componente acido/pronucleofilo per la sintesi di amine da alcoli,
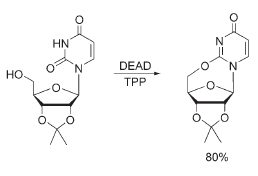
3) versioni intramolecolari,
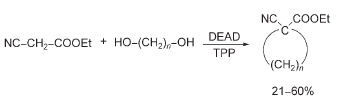
4) selettività per la reazione al centro alcolico primario rispetto al secondario in un diolo,
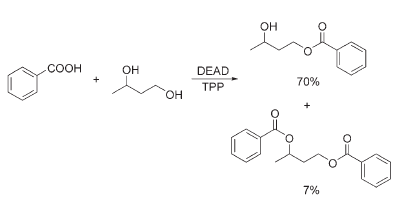
e 5) l'uso di gruppi metilenici attivati quali carboni acidi.

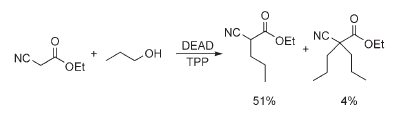
Inoltre, Mitsunobu usò anche la combinazione di DEAD e TPP per convertire le tiouree in carbodiimmine, le tioammidi in chetenimmine, e i tioli in disolfuri.
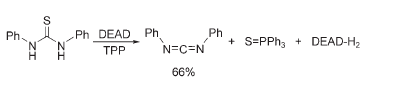
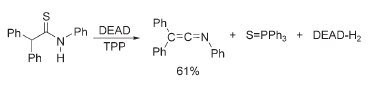
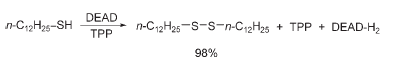
I dettagli meccanicistici di queste ultime reazioni non sono stati riportati; comunque, la funzione della TPP fu scoperta essere solo catalitica, dato che era quindi necessaria ma era intatta alla fine della reazione.
I seguenti utenti ringraziano quimico per questo messaggio: Max Fritz
A causa dell'importanza e dell'uso diffuso della reazione di Mitsunobu, i dettagli del suo meccanismo sono stati ampiamente studiati attraverso una varietà di metodi.
Il meccanismo generalmente accettato oggi con il DEAD e la TPP quali reagenti rappresentativi che possono rendere conto degli esiti osservati sperimentalmente è sottolineato nello schema sottostante.
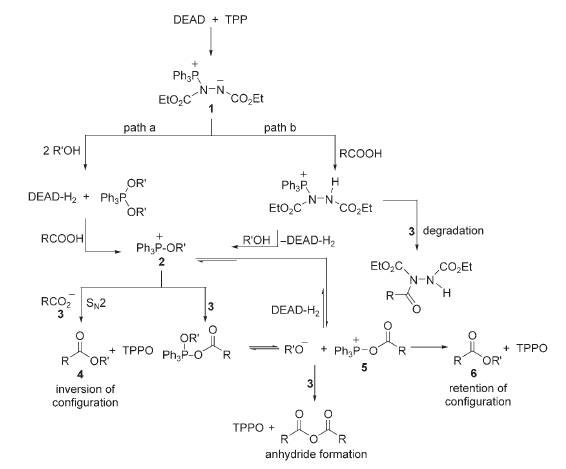
Il primo passaggio nella reazione di Mitsunobu è l'addizione nucleofila della TPP al DEAD a formare la betaina di Morrison–Brunn–Huisgen 1. Questo intermedio reattivo può quindi o reagire con due molecole dell'alcole producendo eventualmente DEAD-H2, la specie alcossifosfonio 2, ed il carbossilato/nucleofilo 3 (path a), o esso può deprotonare l'acido/pronucleofilo a formare eventualmente, di nuovo, DEAD-H2, 2, e 3 (path b). La sostituzione nucleofila del TPPO da 2 a 3
completa la reazione formando il prodotto di coupling 4 che ha stereochimica invertita rispetto al materiale di partenza, l'alcole.
È stata dimostrato che la specie 2 è in equilibrio con la specie
acilossifosfonio 5, e questa specie può, in rari casi, portare al prodotto di coupling 6, che ritiene la stereochimica originale dell'alcole, e alla formazione dell'anidride. La posizione di questo equilibrio è probabilmente mediata dal DEAD-H2 ed è dipendente dalla pKa dell'acido/pronucleofilo, con la specie 2 favorita da composti più acidi. Inoltre, è stato osservato ed è supportato da evidenza sperimentale che, in alcuni casi, la specie 5 può essere formata per prima e quindi convertita nella specie 2. Questo può spiegare perché, quando vengono usati quali substrati di reazione alcuni alcoli secondari molto impiediti stericamente, essi possono favorire la formazione della specie 6, dato che la conversione della specie 5 nella specie 2 può essere sensibili a tensioni steriche.
Per quanto concerne i dettagli e la complessità di questo meccanismo, la formazione della specie 2 è fortemente preferita nella maggior parte dei casi, e l'inversione della stereochimica è correttamente osservata. I casi in cui la specie 5 è favorita e la ritenzione di configurazione viene osservata sono molto rari.
Più recentemente, investigazioni quantomeccaniche (DFT) sulla reazione di Mitsunobu usando PH3 e dimetil azodicarbossilato quali reagenti, rispettivamente, riducente ed ossidante, indicano che il meccanismo può essere in realtà ben più complesso, con equilibri addizionali multipli che competono tra di loro.
Uno dei maggiori svantaggi della reazione di Mitsunobu è che, oltre ai due reagenti, essa richiede l'uso di quantità stechiometriche di due altri reagenti che portano ognuno ad un sottoprodotto.
Quindi, anche in reazioni che sono relativamente efficaci e portano con rese elevato al prodotto desiderato, questo prodotto può essere difficile da isolare dalla miscela di reazione, che può contenere un eccesso di reagenti/reagenti non reagiti e materiali di partenza oltre ai due sottoprodotti. Quindi, molte ricerche sono state indirizzate verso lo sviluppo di alternative al DEAD e alla TPP che facilitassero la purificazione del prodotto desiderato. Riporterò alcune di queste alternative, spesso geniali.
Il reagente basato sulla trifenilfosfina ma legato ad un ferrocenile 7 è stato usato assieme al di-tert-butil azodicarbossilato (8) in
reazioni di Mitsunobu che NON richiedono purificazione cromatografica del prodotto desiderato.
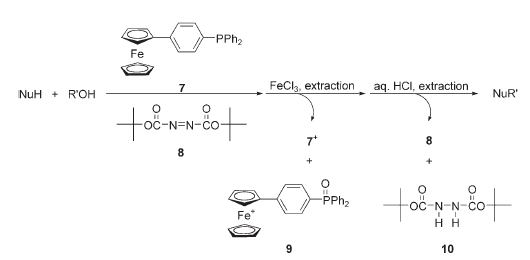 Il gruppo ferrocenile serve come redox-switchable phase tag dato che può essere facilmente ossidato dal FeCl3 ad un catione che è insolubile nei solventi non polari. Dopo la reazione di Mitsunobu con la specie 7, è stato aggiunto FeCl3, e le specie cationiche legate alla specie fosfinica (7+ e 9) quindi formatesi sono state estratte con acqua. Questa estrazione è seguita da trattamento con HCl per decomporre ogni residuo del reagente 8 e del suo sottoprodotto ridotto 10. Tali trattamenti sequenziali hanno permesso l'isolazione diretta del prodotto desiderato con rese praticamente quantitativa con elevata purezza (generalmente >90%). Inoltre, è stato riportato che il reagente 7 potrebbe essere rigenerato tramite riduzione sequenziale di 9 con Na2S2O3 e HSiCl3.
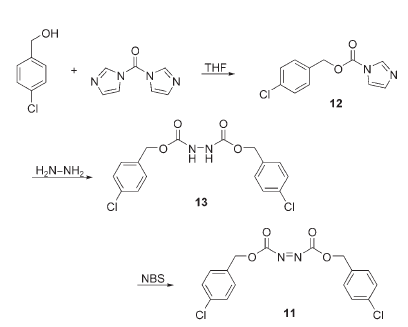
Un'altra alternativa all'azo reagente DEAD è stata recentemente descritta. Il di-4-clorobenzil azodicarbossilato (11) è stato facilmente preparato in tre passaggi attraverso:
1) miscelazione dell'alcole 4-clorobenzilico con l'1,1’-carbonildiimidazolo,
2) reazione del risultante carbammato 12 con idrazina a formare la specie 13, e
3) ossidazione dell'idrazide 13 con N-bromosuccinimide (NBS).
Il gruppo ferrocenile serve come redox-switchable phase tag dato che può essere facilmente ossidato dal FeCl3 ad un catione che è insolubile nei solventi non polari. Dopo la reazione di Mitsunobu con la specie 7, è stato aggiunto FeCl3, e le specie cationiche legate alla specie fosfinica (7+ e 9) quindi formatesi sono state estratte con acqua. Questa estrazione è seguita da trattamento con HCl per decomporre ogni residuo del reagente 8 e del suo sottoprodotto ridotto 10. Tali trattamenti sequenziali hanno permesso l'isolazione diretta del prodotto desiderato con rese praticamente quantitativa con elevata purezza (generalmente >90%). Inoltre, è stato riportato che il reagente 7 potrebbe essere rigenerato tramite riduzione sequenziale di 9 con Na2S2O3 e HSiCl3.
Un'altra alternativa all'azo reagente DEAD è stata recentemente descritta. Il di-4-clorobenzil azodicarbossilato (11) è stato facilmente preparato in tre passaggi attraverso:
1) miscelazione dell'alcole 4-clorobenzilico con l'1,1’-carbonildiimidazolo,
2) reazione del risultante carbammato 12 con idrazina a formare la specie 13, e
3) ossidazione dell'idrazide 13 con N-bromosuccinimide (NBS).
 Il paragone tra la specie 11 e il DEAD in un'ampia varietà di reazioni di Mitsunobu ha dimostrato che sono efficienti allo stesso modo. I vantaggi riportati della specie 11 rispetto al DEAD sono che esso è un solido stabile a temperatura ambiente e la ritenzione del suo sottoprodotto 13 su gel di silice sono distintamente differenti da quelli del DEAD-H2. Inoltre, la specie 13 può essere quasi completamente rimossa dal prodotto della reazione desiderato semplicemente tramite precipitazione con DCM.
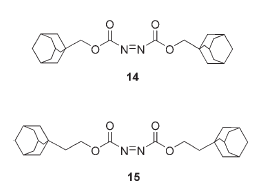
Curran e colleghi riportarono una serie di azo reagenti di nuova concenzione, inclusi una coppia di reagenti legati a ciclodestrina che recavano gruppi adamantile: bis(1-adamantilmetil) azodicarbossilato (14) e bis(2-(1-adamantil)etil) azodicarbossilato (15).
Il paragone tra la specie 11 e il DEAD in un'ampia varietà di reazioni di Mitsunobu ha dimostrato che sono efficienti allo stesso modo. I vantaggi riportati della specie 11 rispetto al DEAD sono che esso è un solido stabile a temperatura ambiente e la ritenzione del suo sottoprodotto 13 su gel di silice sono distintamente differenti da quelli del DEAD-H2. Inoltre, la specie 13 può essere quasi completamente rimossa dal prodotto della reazione desiderato semplicemente tramite precipitazione con DCM.
Curran e colleghi riportarono una serie di azo reagenti di nuova concenzione, inclusi una coppia di reagenti legati a ciclodestrina che recavano gruppi adamantile: bis(1-adamantilmetil) azodicarbossilato (14) e bis(2-(1-adamantil)etil) azodicarbossilato (15).
 Questi reagenti e i loro prodotti corrispondenti ridotti furono trovati avere tempi di ritenzione significativamente più lunghi su gel di silice legato a ciclodestrina rispetto ai tipici prodotti delle reazione di Mitsunobu. Quindi, essi e i loro sottoprodotti potevano essere facilmente separati dal prodotto della reazione desiderato. Furono riportati anche due azo reagenti fluorurati di seconda generazione, 16 ed 17.
Questi reagenti e i loro prodotti corrispondenti ridotti furono trovati avere tempi di ritenzione significativamente più lunghi su gel di silice legato a ciclodestrina rispetto ai tipici prodotti delle reazione di Mitsunobu. Quindi, essi e i loro sottoprodotti potevano essere facilmente separati dal prodotto della reazione desiderato. Furono riportati anche due azo reagenti fluorurati di seconda generazione, 16 ed 17.
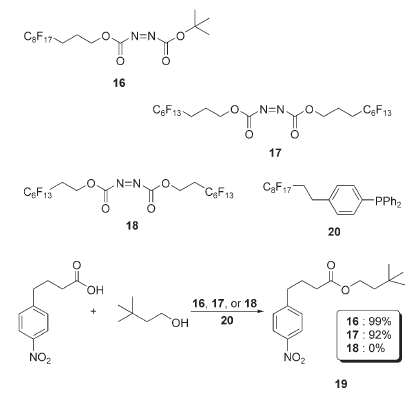 Il reagente di prima generazione 18 fu scoperto essere non così adatto per l'uso nelle reazioni di Mitsunobu che coinvolgevano alcoli stericamente impediti e/o acidi/pronucleofili meno acidi. È stato trovato che gruppi metilenici addizionali che separano le estremità fluorurate e i gruppi azo di 16 ed 17 permettevano loro di essere molto più utili in tali reazioni di Mitsunobu.
Per esempio, la reazione di coupling dell'acido 4-(4-nitrofenil)butirrico con il 3,3-dimetilbutanolo in presenza di 16, 17, o 18, portavano al prodotto desiderato 19 con una resa di 99, 92, e 0%, rispettivamente, quando veniva usato il reagente fosfinico fluorurato 20 quale reagente riducente.
È stato suggerito che la specie 16 è il reagente di scelta quando la purificazione del prodtto deve essere ottenuta con cromatografia a media pressione su fase fluorurata, e che 20 dovrebbe usato quando l'estrazione in fase solida fluorurata viene usata. Più recentemente, una metodologia complementare per l'estrazione liquido-liquido è stata riportata per la purificazione di prodotti di reagenti di Mitsunobu fluorurate con tali reagenti.
In un altro esempio di uso simultaneo di reagenti del tipo appena descritto nelle reazioni di Mitsunobu, i sali di fosfonio sono stati usati per controllare la solubilità dei reagenti e quindi facilitare l'isolamento del prodotto. I sali di tetraarilfosfonio perclorato ed esafluorofosfato sono piuttosto insolubili in dietil etere, e questa proprietà permette loro di essere efficacemente precipitati dalle miscele di reazione in solventi più polari quali il diclorometano tramite addizione di questi solventi.
Per dimostrate l'utilità di tali sali nel facilitare la purificazione del prodotto, i reagenti 21 e 22 sono stati preparati ed usati simultaneamente nelle reazioni di Mitsunobu.
Il reagente di prima generazione 18 fu scoperto essere non così adatto per l'uso nelle reazioni di Mitsunobu che coinvolgevano alcoli stericamente impediti e/o acidi/pronucleofili meno acidi. È stato trovato che gruppi metilenici addizionali che separano le estremità fluorurate e i gruppi azo di 16 ed 17 permettevano loro di essere molto più utili in tali reazioni di Mitsunobu.
Per esempio, la reazione di coupling dell'acido 4-(4-nitrofenil)butirrico con il 3,3-dimetilbutanolo in presenza di 16, 17, o 18, portavano al prodotto desiderato 19 con una resa di 99, 92, e 0%, rispettivamente, quando veniva usato il reagente fosfinico fluorurato 20 quale reagente riducente.
È stato suggerito che la specie 16 è il reagente di scelta quando la purificazione del prodtto deve essere ottenuta con cromatografia a media pressione su fase fluorurata, e che 20 dovrebbe usato quando l'estrazione in fase solida fluorurata viene usata. Più recentemente, una metodologia complementare per l'estrazione liquido-liquido è stata riportata per la purificazione di prodotti di reagenti di Mitsunobu fluorurate con tali reagenti.
In un altro esempio di uso simultaneo di reagenti del tipo appena descritto nelle reazioni di Mitsunobu, i sali di fosfonio sono stati usati per controllare la solubilità dei reagenti e quindi facilitare l'isolamento del prodotto. I sali di tetraarilfosfonio perclorato ed esafluorofosfato sono piuttosto insolubili in dietil etere, e questa proprietà permette loro di essere efficacemente precipitati dalle miscele di reazione in solventi più polari quali il diclorometano tramite addizione di questi solventi.
Per dimostrate l'utilità di tali sali nel facilitare la purificazione del prodotto, i reagenti 21 e 22 sono stati preparati ed usati simultaneamente nelle reazioni di Mitsunobu.
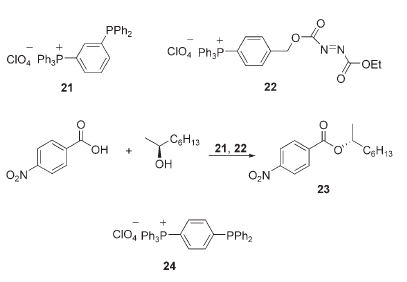 Alla fine delle reazioni, è stato aggiunto del dietil etere per precipitare tutte le specie di sale fosfonio. La successiva filtrazione e concentrazione ha portato al prodotto puro. Questo sistema di reazione è particolarmente efficiente dato che solo 1.5 equivalenti sia di 21 che di 22 sono stati necessari per ottenere con elevate rese 23. Curiosamente, il reagente isomero 24 è stato riportato essere sostanzialmente meno reattivo in queste reazioni rispetto al 21.
Alla fine delle reazioni, è stato aggiunto del dietil etere per precipitare tutte le specie di sale fosfonio. La successiva filtrazione e concentrazione ha portato al prodotto puro. Questo sistema di reazione è particolarmente efficiente dato che solo 1.5 equivalenti sia di 21 che di 22 sono stati necessari per ottenere con elevate rese 23. Curiosamente, il reagente isomero 24 è stato riportato essere sostanzialmente meno reattivo in queste reazioni rispetto al 21.
I seguenti utenti ringraziano quimico per questo messaggio: Max Fritz, None
È stato ripotato l'uso simultaneo di due analoghi del DEAD e della TPP supportati su polimero in reazioni di Mitsunobu. I reagenti 25 e 26, derivati da una reazione di ring-opening
metathesis polymerization (ROMP), sono stati preparati dai corrispondenti monomeri del norbornene.
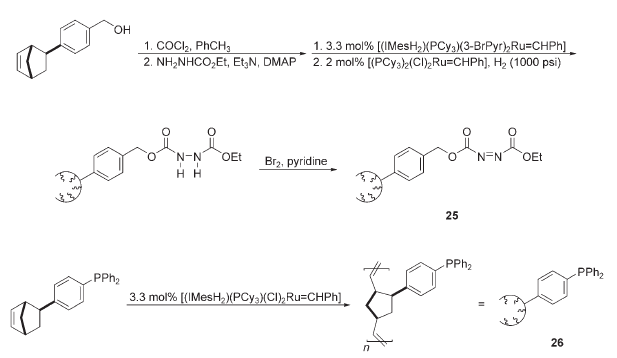
Questi potrebbero esser usati assieme in reazioni di Mitsunobu per formare la specie betainica reattiva richiesta a causa della loro solubilità in THF, e potrebbero essere rimossi dalla miscela di reazione basandosi sulla loro insolubilità in EtOAc. Per esempio, la reazione tra il 4-NBA ed il 3-fenilpropanolo ha prodotto l'estere desiderato con rese elevate quando 2 equiv. di entrambi i 25 e 26 venivano usati. Alla fine della reazione, l'eccesso di 25 e 26 ed i sottoprodotti supportati sul polimero venivano rimossi tramite precipitazione e filtrazione. Da notare che, sebbene siano stati riportati molti esempi sull'uso di fosfine ed azo reagenti supportati su polimero in reazioni di Mitsunobu, la loro natura eterogenea preclude l'uso di tali reagenti assieme. Tali reazioni di Mitsunobu multipolimero sono possibili solo quando almeno uno dei reagenti supportati su polimero è presente come parte della miscela di reazione omogenea.
In una maniera simile, i reagenti 27 e 28 supportati su poligliceroli, solubili ed alto PM sono stai usati simultaneamente in reazioni di Mitsunobu.
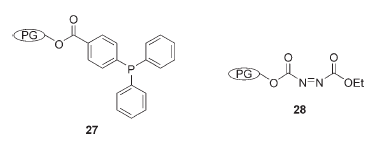
Il poliglicerolo usato come materiale di supporto è stato preparato tramite la polimerizzazione ionica del glicidolo ed ha una struttura dendritica.
Nelle reazioni di Mitsunobu riportate con questi reagenti, tutti i reagenti polimerici e i sottoprodotti sono stati rimossi tramite una semplice procedura di precipitazione/filtrazione a dare prodotti ad elevata purezza senza dover ricorrere a separazione cromatografica.
Tsunoda e colleghi hanno recentemente pubblicato i dettagli della preparazione e dell'uso dei loro precedentemente riportati reagenti cianometilenetrimetilfosforano (29) e cianometilenetributilfosforano (30), che possono effettuare reazioni di Mitsunobu per loro conto.
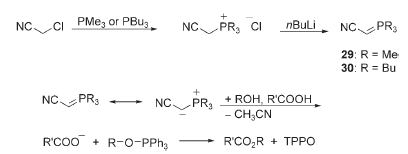
I reagenti 29 e 30 sono stati sintetizzati in due passaggi da cloroacetonitrile e dall'appropriata trialchilfosfina, e sono utili nel partecipare a reazioni di Mitsunobu in cui l'acido/pronucleofilo di partenza ha pKa>13. Inoltre, 29 e 30 sono a quanto riportato gli unici reagenti che possono essere effettivamente applicati in reazioni di Mitsunobu di sulfonammidi non sostituite all'atomo di azoto come la p-toluenesulfonammide. I reagenti 29 e 30 sono molto sensibili a luce e umidità; quindi, essi dovrebbero essere conservati ed usati con molta attenzione.
In un lavoor correlato alla reazione di Mitsunobu, Mukaiyama et al. hanno continuato la loro ricerca nelle reazioni di condensazione tramite ossidazione–riduzione e recentemente hanno riportato l'uso del chinone sostituito 31 quale ossidante in tali reazioni.
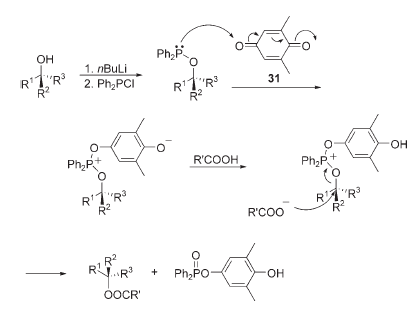
In queste reazioni, un'alcossidifenilfosfina generata in situ reagisce con un acido carbossilico in presenza di 31 a dare un estere con stereochimica al centro alcolico invertita in condizioni neutre. Questa reazione di sostituzione procede anche quando viene usato un alcole terziario. Inoltre, quando viene usato un alcole al posto dell'acido carbossilico, si forma un etere.
Recentemente, l'attenzione è stata concentrata altrove rispetto allo sviluppo di reagenti alternativi per facilitare la purificazione dei prodotti della reazione di Mitsunobu spostandola verso l'identificazione di nuove procedure di reazione e nuovi protocolli di workup che portassero allo stesso risultato. Questo è probabilmente dovuto al fatto che la maggior parte dei reagenti alternativi riportati in letteratura non sono commercialmente disponibili e richiedono sequenze di sintesi multistep per la loro preparazione. A questo riguardo, è stato riportato che i prodotti puri di reazione della Mitsunobu possono essere ottenuti attraverso, per prima cosa, lavaggio della miscela di reazione grezza con una soluzione di perossido di idrogeno al 15% in peso, seguito da aggiunta di una soluzione acquosa di sodio solfito (per ridurre ogni perossido residuo), e quindi filtrazione attraverso gel di silice. Il lavaggio ossidativo converte ogni fosfina residua nel corrispondente ossido, che è molto polare. Con questo protocollo, il prodotto puro è stato ottenuto con una resa del 96% dalla reazione dell'N-idrossiftalimmide con alcole prenilico su una scala di 20 grammi.
È stata riportata la prima versione della reazione di Mitsunobu che è catalitica nell'ossidante (DEAD). Questo sistema di reazione utilizza lo iodosobenzene diacetato (32) quale ossidante stechiometrico, che riduce il ruolo del DEAD a quello di catalizzatore.
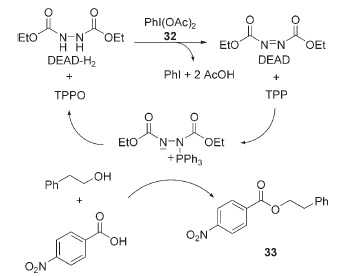
In questo modo, la purificazione del prodotto è facilitata dalla riduzione della richiesta quantità di un reagente che produce un sottoprodotto che è difficile da rimuovere.
Per esempio, la reazione del 4-NBA e del 2-feniletanolo con 0.1 equiv. di DEAD e 2 equiv. sia di TPP che di 32 ha fornito il prodotto desiderato 33 con una resa del 90%.
Fino ad oggi, che io sappia, non è stata riportata alcuna versione della reazione di Mitsunobu che è catalitica o in TPP o in un surrogato per il reagente riducente fosfinico, e lo sviluppo di un tale sistema di reazione rimane una delle sfide chiave in questo campo.
I seguenti utenti ringraziano quimico per questo messaggio: None, NaClO














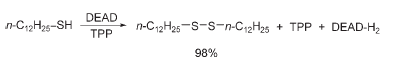

 Il gruppo ferrocenile serve come redox-switchable phase tag dato che può essere facilmente ossidato dal FeCl3 ad un catione che è insolubile nei solventi non polari. Dopo la reazione di Mitsunobu con la specie 7, è stato aggiunto FeCl3, e le specie cationiche legate alla specie fosfinica (7+ e 9) quindi formatesi sono state estratte con acqua. Questa estrazione è seguita da trattamento con HCl per decomporre ogni residuo del reagente 8 e del suo sottoprodotto ridotto 10. Tali trattamenti sequenziali hanno permesso l'isolazione diretta del prodotto desiderato con rese praticamente quantitativa con elevata purezza (generalmente >90%). Inoltre, è stato riportato che il reagente 7 potrebbe essere rigenerato tramite riduzione sequenziale di 9 con Na2S2O3 e HSiCl3.
Un'altra alternativa all'azo reagente DEAD è stata recentemente descritta. Il di-4-clorobenzil azodicarbossilato (11) è stato facilmente preparato in tre passaggi attraverso:
1) miscelazione dell'alcole 4-clorobenzilico con l'1,1’-carbonildiimidazolo,
2) reazione del risultante carbammato 12 con idrazina a formare la specie 13, e
3) ossidazione dell'idrazide 13 con N-bromosuccinimide (NBS).
Il gruppo ferrocenile serve come redox-switchable phase tag dato che può essere facilmente ossidato dal FeCl3 ad un catione che è insolubile nei solventi non polari. Dopo la reazione di Mitsunobu con la specie 7, è stato aggiunto FeCl3, e le specie cationiche legate alla specie fosfinica (7+ e 9) quindi formatesi sono state estratte con acqua. Questa estrazione è seguita da trattamento con HCl per decomporre ogni residuo del reagente 8 e del suo sottoprodotto ridotto 10. Tali trattamenti sequenziali hanno permesso l'isolazione diretta del prodotto desiderato con rese praticamente quantitativa con elevata purezza (generalmente >90%). Inoltre, è stato riportato che il reagente 7 potrebbe essere rigenerato tramite riduzione sequenziale di 9 con Na2S2O3 e HSiCl3.
Un'altra alternativa all'azo reagente DEAD è stata recentemente descritta. Il di-4-clorobenzil azodicarbossilato (11) è stato facilmente preparato in tre passaggi attraverso:
1) miscelazione dell'alcole 4-clorobenzilico con l'1,1’-carbonildiimidazolo,
2) reazione del risultante carbammato 12 con idrazina a formare la specie 13, e
3) ossidazione dell'idrazide 13 con N-bromosuccinimide (NBS).
 Il paragone tra la specie 11 e il DEAD in un'ampia varietà di reazioni di Mitsunobu ha dimostrato che sono efficienti allo stesso modo. I vantaggi riportati della specie 11 rispetto al DEAD sono che esso è un solido stabile a temperatura ambiente e la ritenzione del suo sottoprodotto 13 su gel di silice sono distintamente differenti da quelli del DEAD-H2. Inoltre, la specie 13 può essere quasi completamente rimossa dal prodotto della reazione desiderato semplicemente tramite precipitazione con DCM.
Curran e colleghi riportarono una serie di azo reagenti di nuova concenzione, inclusi una coppia di reagenti legati a ciclodestrina che recavano gruppi adamantile: bis(1-adamantilmetil) azodicarbossilato (14) e bis(2-(1-adamantil)etil) azodicarbossilato (15).
Il paragone tra la specie 11 e il DEAD in un'ampia varietà di reazioni di Mitsunobu ha dimostrato che sono efficienti allo stesso modo. I vantaggi riportati della specie 11 rispetto al DEAD sono che esso è un solido stabile a temperatura ambiente e la ritenzione del suo sottoprodotto 13 su gel di silice sono distintamente differenti da quelli del DEAD-H2. Inoltre, la specie 13 può essere quasi completamente rimossa dal prodotto della reazione desiderato semplicemente tramite precipitazione con DCM.
Curran e colleghi riportarono una serie di azo reagenti di nuova concenzione, inclusi una coppia di reagenti legati a ciclodestrina che recavano gruppi adamantile: bis(1-adamantilmetil) azodicarbossilato (14) e bis(2-(1-adamantil)etil) azodicarbossilato (15).
 Questi reagenti e i loro prodotti corrispondenti ridotti furono trovati avere tempi di ritenzione significativamente più lunghi su gel di silice legato a ciclodestrina rispetto ai tipici prodotti delle reazione di Mitsunobu. Quindi, essi e i loro sottoprodotti potevano essere facilmente separati dal prodotto della reazione desiderato. Furono riportati anche due azo reagenti fluorurati di seconda generazione, 16 ed 17.
Questi reagenti e i loro prodotti corrispondenti ridotti furono trovati avere tempi di ritenzione significativamente più lunghi su gel di silice legato a ciclodestrina rispetto ai tipici prodotti delle reazione di Mitsunobu. Quindi, essi e i loro sottoprodotti potevano essere facilmente separati dal prodotto della reazione desiderato. Furono riportati anche due azo reagenti fluorurati di seconda generazione, 16 ed 17.
 Il reagente di prima generazione 18 fu scoperto essere non così adatto per l'uso nelle reazioni di Mitsunobu che coinvolgevano alcoli stericamente impediti e/o acidi/pronucleofili meno acidi. È stato trovato che gruppi metilenici addizionali che separano le estremità fluorurate e i gruppi azo di 16 ed 17 permettevano loro di essere molto più utili in tali reazioni di Mitsunobu.
Per esempio, la reazione di coupling dell'acido 4-(4-nitrofenil)butirrico con il 3,3-dimetilbutanolo in presenza di 16, 17, o 18, portavano al prodotto desiderato 19 con una resa di 99, 92, e 0%, rispettivamente, quando veniva usato il reagente fosfinico fluorurato 20 quale reagente riducente.
È stato suggerito che la specie 16 è il reagente di scelta quando la purificazione del prodtto deve essere ottenuta con cromatografia a media pressione su fase fluorurata, e che 20 dovrebbe usato quando l'estrazione in fase solida fluorurata viene usata. Più recentemente, una metodologia complementare per l'estrazione liquido-liquido è stata riportata per la purificazione di prodotti di reagenti di Mitsunobu fluorurate con tali reagenti.
In un altro esempio di uso simultaneo di reagenti del tipo appena descritto nelle reazioni di Mitsunobu, i sali di fosfonio sono stati usati per controllare la solubilità dei reagenti e quindi facilitare l'isolamento del prodotto. I sali di tetraarilfosfonio perclorato ed esafluorofosfato sono piuttosto insolubili in dietil etere, e questa proprietà permette loro di essere efficacemente precipitati dalle miscele di reazione in solventi più polari quali il diclorometano tramite addizione di questi solventi.
Per dimostrate l'utilità di tali sali nel facilitare la purificazione del prodotto, i reagenti 21 e 22 sono stati preparati ed usati simultaneamente nelle reazioni di Mitsunobu.
Il reagente di prima generazione 18 fu scoperto essere non così adatto per l'uso nelle reazioni di Mitsunobu che coinvolgevano alcoli stericamente impediti e/o acidi/pronucleofili meno acidi. È stato trovato che gruppi metilenici addizionali che separano le estremità fluorurate e i gruppi azo di 16 ed 17 permettevano loro di essere molto più utili in tali reazioni di Mitsunobu.
Per esempio, la reazione di coupling dell'acido 4-(4-nitrofenil)butirrico con il 3,3-dimetilbutanolo in presenza di 16, 17, o 18, portavano al prodotto desiderato 19 con una resa di 99, 92, e 0%, rispettivamente, quando veniva usato il reagente fosfinico fluorurato 20 quale reagente riducente.
È stato suggerito che la specie 16 è il reagente di scelta quando la purificazione del prodtto deve essere ottenuta con cromatografia a media pressione su fase fluorurata, e che 20 dovrebbe usato quando l'estrazione in fase solida fluorurata viene usata. Più recentemente, una metodologia complementare per l'estrazione liquido-liquido è stata riportata per la purificazione di prodotti di reagenti di Mitsunobu fluorurate con tali reagenti.
In un altro esempio di uso simultaneo di reagenti del tipo appena descritto nelle reazioni di Mitsunobu, i sali di fosfonio sono stati usati per controllare la solubilità dei reagenti e quindi facilitare l'isolamento del prodotto. I sali di tetraarilfosfonio perclorato ed esafluorofosfato sono piuttosto insolubili in dietil etere, e questa proprietà permette loro di essere efficacemente precipitati dalle miscele di reazione in solventi più polari quali il diclorometano tramite addizione di questi solventi.
Per dimostrate l'utilità di tali sali nel facilitare la purificazione del prodotto, i reagenti 21 e 22 sono stati preparati ed usati simultaneamente nelle reazioni di Mitsunobu.
 Alla fine delle reazioni, è stato aggiunto del dietil etere per precipitare tutte le specie di sale fosfonio. La successiva filtrazione e concentrazione ha portato al prodotto puro. Questo sistema di reazione è particolarmente efficiente dato che solo 1.5 equivalenti sia di 21 che di 22 sono stati necessari per ottenere con elevate rese 23. Curiosamente, il reagente isomero 24 è stato riportato essere sostanzialmente meno reattivo in queste reazioni rispetto al 21.
Alla fine delle reazioni, è stato aggiunto del dietil etere per precipitare tutte le specie di sale fosfonio. La successiva filtrazione e concentrazione ha portato al prodotto puro. Questo sistema di reazione è particolarmente efficiente dato che solo 1.5 equivalenti sia di 21 che di 22 sono stati necessari per ottenere con elevate rese 23. Curiosamente, il reagente isomero 24 è stato riportato essere sostanzialmente meno reattivo in queste reazioni rispetto al 21.



