quimico
2012-11-24 09:23
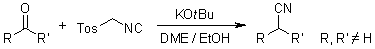
La reazione di Van Leusen permette la conversione di un chetone in un nitrile con un atomo di carbonio in più in un singolo passaggio usando il tosilmetil isonitrile (TosMIC) quale sintone.
Meccanismo
Il TosMIC, come già da me accennato, è un sintone C1 unico che può essere facilmente deprotonato e alchilato. Il gruppo sulfinile non solo aumenta l'acidità dei protoni in α, ma è anche un buon gruppo uscente. In aggiunta, il TosMIC raggruppa le uniche proprietà del gruppo isonitrile in cui l'ossidazione dell'atomo di carbonio è una driving force per reazioni multiple.
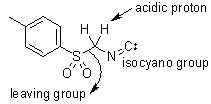
Per esempio, il TosMIC può essere usato come un sintone C-N=C per la sintesi di diversi eterocicli, come gli ossazoli (* Sintesi ossazolica di Van Leusen), gli imidazoli (° Sintesi imidazolica di Van Leusen), pirroli, 1,2,4-triazoli e molti altri.
La conversione dei chetoni negli omologhi nitrili può anche essere formalmente descritta come una "nitrilazione riduttiva, dato che dopo l'addizione del TosMIC al chetone, il risultante gruppo α-idrossi è rimosso. Anzi, l'atomo di carbonio del gruppo isonitrile viene ossidato nel corso della reazione.
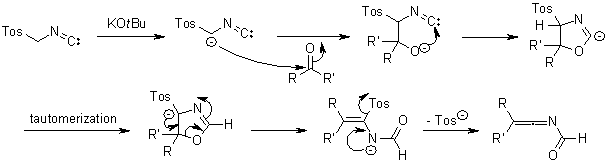
Nella formazione del nitrile, la forma deprotonata dell'alcole che è stato aggiunto alla miscela di reazione ora gioca un ruolo cruciale dato che è un nucleofilo nella deformilazione della chetimmina:
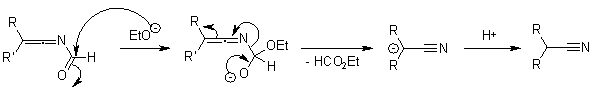
Sebbene la reazione possa tuttavia portare a nitrili senza l'aggiunta di un alcole primario, il processo è considerevolmente velocizzato in presenza di MeOH o EtOH. Sfortunatamente, l'uso di un eccesso di un alcole primario favorisce anche la formazione di una 4-alcossi-2-ossazolina, così che la quantità di alcole primario deve essere controllata giudiziosamente - tipicamente nel range di 1-2 equivalenti.
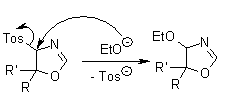
Per una dettagliata discussione meccanicistica, guardare la pubblicazione di Van Leusen (J. Org. Chem., 1977, 42, 3114-3118).
* Sintesi ossazolica di Van Leusen
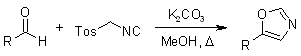
La sintesi ossazolica di Van Leusen permette la preparazione di ossazoli da aldeidi tramite reazione con il TosMIC.
Meccanismo
La reazione è guidata dalla reattività unica del TosMIC, come già spiegato/detto.
Dopo l'aggiunta del TosMIC deprotonato all'aldeide e la formazione del legame tra il risultante gruppo idrossi e il gruppo isonitrile, si ottiene una ossazolina come intermedio:
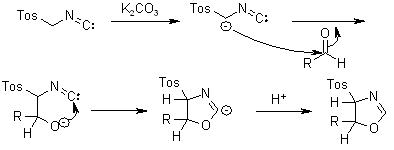
A differenza della reazione di Van Leusen (sintesi di nitrili da chetoni), l'esistenza di un protone in posizione β al gruppo sulfinile permette una eliminazione promossa da base:
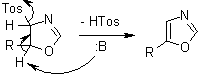
Un meccanismo può essere trovato in una pubblicazione di Van Leusen (Tetrahedron Lett., 1972, 13, 3114-3118).
La formazione in situ di aldimmine tramite reazione di aldeidi e di un'amina, e la successiva reazione con il TosMIC, permette una sintesi di imidazoli (vd. sotto).
° Sintesi imidazolica di Van Leusen o reazione a tre componenti di Van Leusen (vL-3CR)
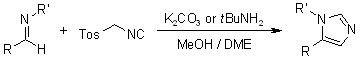
La sintesi imidazolica di Van Leusen permette la preparazione di imidazoli da aldimmine tramite reazione col TosMIC. La reazione è stata precedentemente espansa ad una sintesi in due passaggi in cui l'aldimmina veniva generata in situ: la Reazione a 3 Componenti di Van Leusen (vL-3CR).
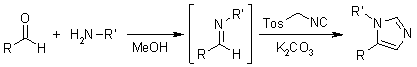
Meccanismo
Il meccanismo in accordo con una pubblicazione di Van Leusen (J. Org. Chem., 1977, 42, 1153-1159) è guidato dal TosMIC.
La terminazione CH2N=C può subire una cicloaddizione per gradi ad un doppio legame polarizzato in condizioni basiche.
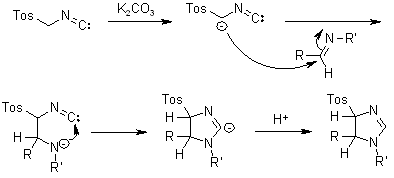
L'eliminazione di acido p-toluenesulfinico (TosH) dall'intermedio 4-tosil-2-imidazolina porta ad un imidazolo 1,5-disostituito:
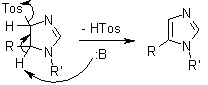
L'aldimmina può essere anche generata in situ tramite condensazione di un'amina con un aldeide in circa 30 minuti. L'acqua formatasi come sottoprodotto non interferisce con la cicloaddizione, e l'aggiunta di agenti disidratanti quale il MgSO4 non è necessaria. Comunque, a dispetto del nome, la vL-3CR non è un vera reazione multicomponente, dato che i componenti reagiscono per gradi.
I seguenti utenti ringraziano quimico per questo messaggio: rock.angel, Dott.MorenoZolghetti, oberon