quimico
2011-12-07 12:05
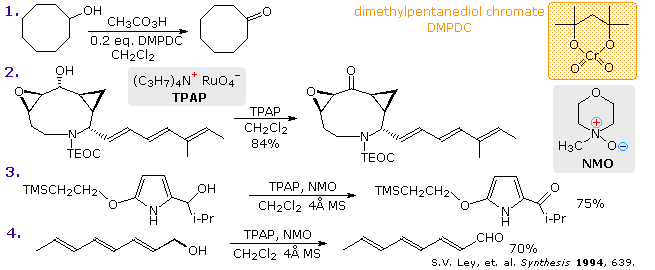
Due reagenti comunemente usati per l'ossidazione di alcoli primari e secondari sono PCC (piridinio clorocromato, C5H5NH+CrO3Cl–) e PDC (piridinio dicromato, (C5H5NH+)2Cr2O7–2).
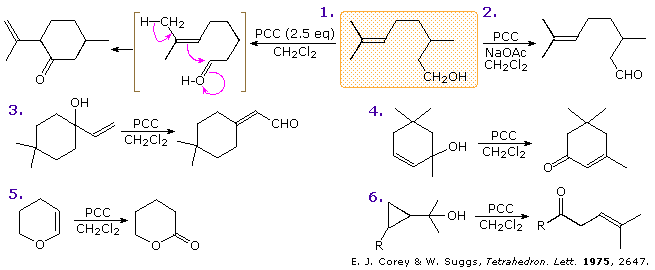
Gli schemi seguenti mostrano alcune reazioni selettive e sinteticamente utili che questi ossidanti possono realizzare. Il primo mostra le reazioni con PCC, mentre il secondo quelle con PDC. La natura aggressiva del PCC è evidente negli esempi 1, 3, 4 & 6. A causa della sua natura acida, il PCC può indurre ciclizzazione di un alchene vicino (1), riarrangiamento di alcoli terziari allilici (3 & 4), o un riarrangiamento equivalente con apertura d'anello di anelli tensionati (6). Il tampone con sodio acetato aiuta a ridurre gli eventi correlati alla sua acidità, come nell'esempio 2. In assenza di funzioni sensibili, questo reagente è la scelta migliore per la conversione semplice di alcoli ad aldeidi e chetoni.
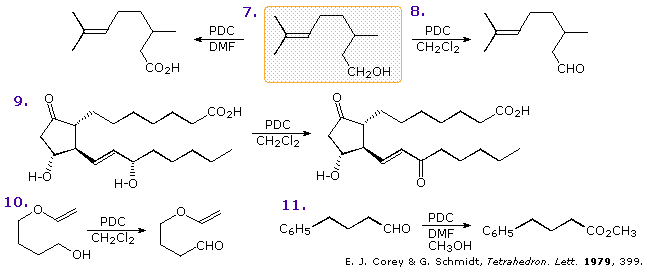
Il PDC un ossidante più blando e più selettivo, come mostrano gli esempi sopra. Come regola, le ossidazioni con PDC sono più lente e possono essere catalizzate da alcune gocce di acido acetico. Gli alcoli allilici sono ossidati più velocemente dei corrispondenti composti saturi, come evidenziato dalla prostaglandina nella reazione 9. Un curioso effetto solvente è osservato per le ossidazioni con PDC. In cloruro di metilene la reazioni di alcoli primari e secondari procede come previsto ma lentamente (8 & 10). In DMF (N,N-dimetilformammide) gli alcoli primari sono ossidati ad acidi carbossilici (7), e con l'aggiunta di alcole ad esteri (11). La natura blanda di questo reagente è dimostrata dalla sopravvivenza del sensibile gruppo enol etere nella reazione 10.
Ossidazione di alcoli tramite DMSO
Ne avevo già parlato ma fa bene riprendere l'argomento.
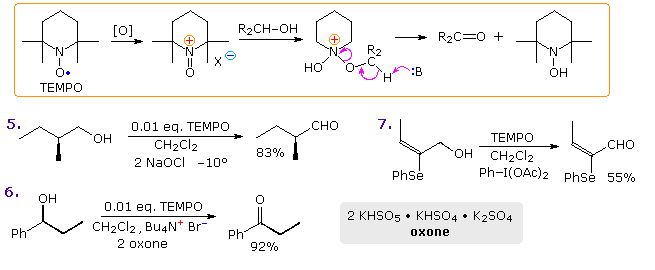
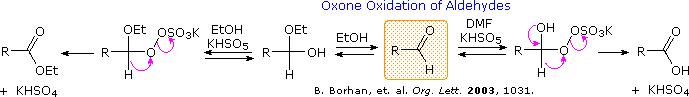
La conversione di alcoli primari e secondari ad aldeidi e chetoni, nella sua forma più semplice, può essere considerata una deidrogenazione (perdita di H2). Fornendo una fonte di ossigeno per fissare l'idrogeno prodotto come acqua, il processo endotermico di deidrogenazione può essere convertito in uno esotermico più favorevole. Una fonte di ossigeno che si è dimostrata efficace per l'ossidazione di alcoli è il semplice solvente solfossido, DMSO. La reazione è semplice dal punto di vista operativo: una soluzione in DMSO dell'alcole è trattata con uno dei diversi reagenti elettrofili disidratanti (E). L'alcole viene ossidato; il DMSO è ridotto a dimetil solfuro; e l'acqua è catturata dall'elettrofilo. Una base aminica come la trietilamina o la piridina è di solito presente in quantità equimolare. A causa della natura esotermica della reazione, essa è di solito condotta a -50 °C o meno. I co-solventi come il cloruro di metilene o il THF sono necessari, in quanto il DMSO puro congela a 18 °C. Sebbene il sotto prodotto dimetil solfuro abbia odore spiacevole, esso è facilmente reso inoffensivo tramite ossidazione con sodio ipoclorito.
Un meccanismo generale plausibile per questa interessante ed utile reazione è disegnato sotto.
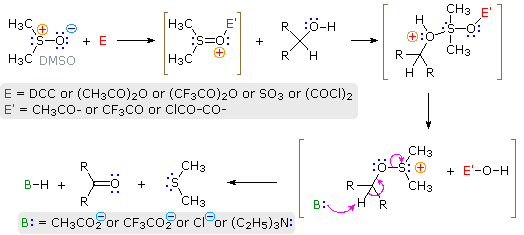
Dato che così tanti elettrofili differenti sono stati usati per fare questa ossidazione, è irragionevole proporre un meccanismo singolo, universale.
La maggior parte degli elettrofili sono buoni agenti acilanti, così uno può aspettarsi una acilazione iniziale dell'ossigeno del solfossido. L'acilazione auemtan il carattere elettrofilo dell'atomo di zolfo. Quindi segue il legame dello zolfo attivato all'atomo di ossigeno dell'alcole. I rimanenti passaggi sono eliminazione, simili per natura a quelli proposti per altre ossidazioni di alcoli.
Il protocollo più comunemente usato per fare un'ossidazione con il DMSO è noto come ossidazione di Swern. In questa procedura l'ossalile cloruro reagisce con il DMSO a bassa temperatura formando il clorodimetilsolfonio cloruro, (CH3)2SCl+ Cl–, che è la specie reattiva che ossida l'alcole. Sotto è riportato un meccanismo per questa ossidazione. Sono state proposte diverse variazioni della eliminazione finale, e due sono mostrate tra parentesi.
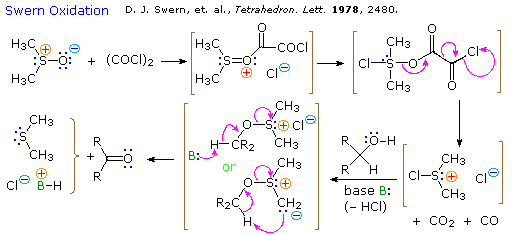
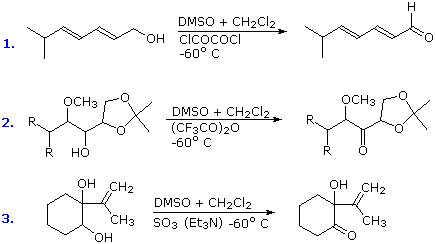
Tre esempi di queste ossidazioni con DMSO sono riportate nello schema che segue. Notate che questa procedura di ossidazione è davvero blanda e tollera una varietà di altri gruppi funzionali, inclusi quelli aventi atomi di azoto e zolfo ossidabili.
Ossidazioni con il periodinano di Dess-Martin
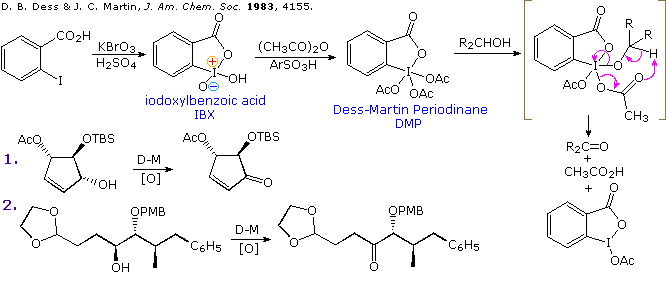
I composti dello iodo ipervalente si sono dimostrati essere efficaci reagenti ossidanti. Tra i più comunemente usati c'è il DMP, la cui preparazione da acido o-iodobenzoico è mostrata nella parte alta dello schema seguente.
L'alcole da ossidare è semplicemente miscelato con il periodinano in soluzione di cloruro di metilene e posto sotto agitazione a temperatura ambiente. Gli alcoli primari portano ad aldeidi e gli alcoli secondari a chetoni. Il reagente e le condizioni sono tolleranti nei confronti di molte funzioni sensibili, quali gli acetali ed i silil eteri. Due esempi sono mostrati nello schema. Un meccanismo plausibile è disegnato sulla destra. Gli svantaggi principali della procedura di Dess-Martin sono il carattere esplosivo dell'intermedio IBX ed il costo commerciale del DMP, assumendo che l'utente non desideri prepararselo.
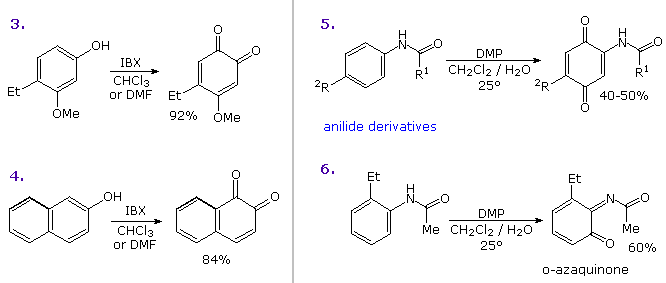
La specie iodossile più sensibile (IBX) può essere direttamente usata come ossidante, ma è relativamente insolubile in solventi non polari. Nonostante ciò, è stato usato per preparare o-chinoni da fenoli para-sostituiti, come mostrato negli esempi 3 e 4. Dato che gli o-chinoni sono abbastanza reattivi, essi non sono normalmente isolati, ma sono usati in situ per diverse reazioni successive. Chinoni ed azachinoni sono stati anche sintetizzati da anilidi per ossidazione con DMP in solventi misti, esempi 5 e 6. In tutti questi casi il substrato deve avere anelli aromatici elettron ricchi, e questo metodo fornisce un'utile alternativa alle ossidazioni con il sale di Fremy, K2NO(SO3)2.
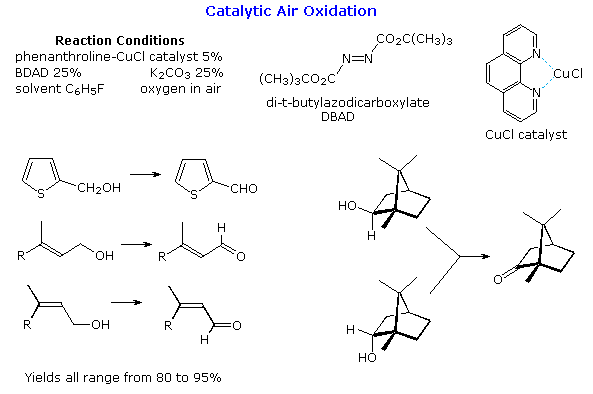
Ossidazione selettiva di alcoli allilici e benzilici
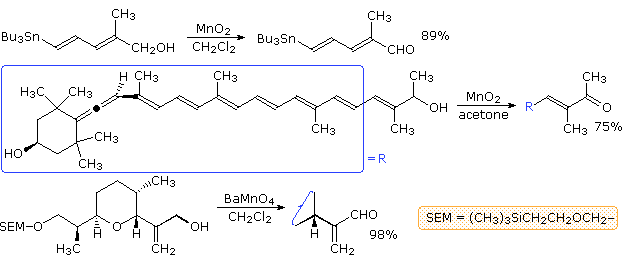
Gli alcoli allilici e benzilici possono essere ossidati selettivamente tramite una sospensione di diossido di manganese attivato in solventi organici adatti. Due esempi sono mostrati sotto. Ossidazioni simili sono state fatte tramite bario permanganato, come mostrato nel terzo esempio.
I seguenti utenti ringraziano quimico per questo messaggio: Nico