quimico
2012-06-21 20:45
Ogni tanto ritorno 
Quello che scrivo è spesso preso dalla rete dai libri e da mie dispense. Difficile quindi riportare ogni riferimenti. Cosa che tra l'altro faccio sempre.
Vorrei parlare di una tipologia di reazioni che conosco da 1po' ma che di questi tempi sto riconsiderando, vuoi per lavoro vuoi per passione per la chimica.
In chimica, una reazione multi-componente (o MCR dall'eng Multi-Component Reaction o talvolta MCAP = "Multi-component Assembly Process" , è una reazione chimica dove tre o più composti reagiscono a formare un singolo prodotto. Per definizione, le reazioni multicomponente sono quelle reazioni in cui più di due reagenti si combinano in maniera sequenziale a dare prodotto estremamente selettivi che ritengono la maggior parte degli atomi dei prodotti di partenza.
, è una reazione chimica dove tre o più composti reagiscono a formare un singolo prodotto. Per definizione, le reazioni multicomponente sono quelle reazioni in cui più di due reagenti si combinano in maniera sequenziale a dare prodotto estremamente selettivi che ritengono la maggior parte degli atomi dei prodotti di partenza.
Sono note da più di 150 anni. La prima sintesi di questo tipo, documentata, fu la sintesi di Strecker di α-amino nitrili nel 1850. Oggi esiste una moltitude di questo tipo di reazioni, e sicuramente le più documentate sono quelle che vedono come reagente comune gli isonitrili. Altre sono mediate da radicali liberi o stabili, altre sono basate su composti organoboro e altre ancora sono catalizzate da metalli.
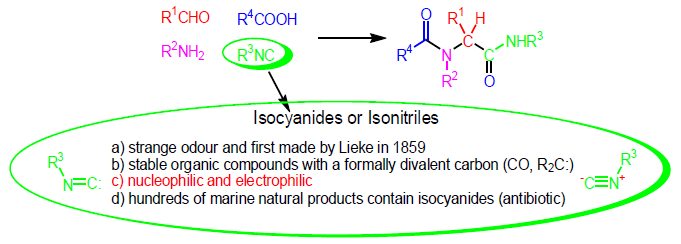
Vi chiedere perché le reazioni multicomponente più frequentemente utilizzate siano quelle basate sugli isonitrili... Beh gli isonitrili sono un gruppo funzionale straordinario (anche se puzzano in modo pauroso). Si ritiene che essi esibiscano risonanza tra le loro forme di carbonio tetravalente e divalente. Questo induce il gruppo isonitrile a subire sia reazioni elettrofile sia reazioni nucleofile all'atomo di carbonio CII, il quale quindi si converte nella sua forma CIV in una reazione esotermica. Anche la presenza di tali composti nei prodotti naturali ha contribuito a rendere questo gruppo funzionale molto utile.
Le due più importanti reazioni multicomponente basate sugli isonitrili sono la reazione di Passerini (è una reazione a 3 componenti che porta alla formazione di α-acilossi carbossammidi) e la sintesi di Ugi (è una reazione a 4 componenti che porta alla formazione di α-acilamino carbossammidi).
Altre reazioni di questo tipo sono ad esempio la trimerizzazione di alchini, la reazioni di Biginelli, la sintesi di Hantzsch della piridina, la reazioni di Mannich, la reazione di Pauson–Khand.
L'esatta natura di queste reazioni è difficile da valutare. Per lo più sono reazioni che coinvolgono processi bimolecolari.
La reazioni di Passerini fu scoperta da Passerini nel 1921 (Passerini, M. Gazz. Chim. Ital. 1921, 51, 126) ed è una reazione a tre componenti: un'aldeide (o un chetone) + un acido carbossilico + un isonitrile.

Questa reazione offre il diretto accesso alle α-idrossi carbossammidi.
Per quanto concerne il meccanismo la reazione di Passerini procede rapidamente se la reazione è condotta in solventi aprotici a temperatura ambiente. Si ottengono rese elevate con elevate concentrazioni dei reagenti di partenza nella miscela di reazione.
Da queste scoperte, è stato assunti che la reazione di Passerini non segue un cammino di reazione ionico. Si ritiene che il legame a idrogeno giochi un ruolo cruciale nella formazione dello stato di transizione ciclico proposto per questa reazione.
Quello riportato è uno dei possibili meccanismi di reazione, in quanto si dibatte ancora oggi su quale sia il vero meccanismo.

Quello che si può dire per certo è che è una reazione che segue una cinetica del terzo ordine, primo ordine per quanto concerne ogni reagente singolo (Baker, R.H., Stanonis, D. J. Am. Chem. Soc. 1951, 73, 699). Come detto Ugi dimostrò che la reazione è accelerata dall'uso di solventi aprotici (il che indica un meccanismo non ionico): basti vedere Ugi, I., Meyr, R., Chem. Ber. 1961, 94, 2229.
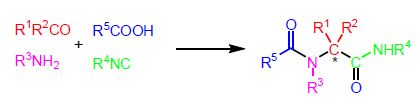
La reazione di Ugi fu scoperta da Ugi nel 1959 (Ugi, I., et. al. Angew. Chem. 1959, 71, 386) ed è una reazione di condensazione a quattro componenti (U-4CC) tra un'aldeide, un'amina, un acido carbossilico ed un isonitrile che permette la rapida preparazione di derivati α-aminoacil ammidici. I prodotti della reazione di Ugi posso esemplificare un vasto range di di modelli di sostituzione, e costituiscono i peptidomimetici che hanno potenziali applicazioni in campo farmacologico. Questa reazione è altresì molto importante per la creazioni di librerie di composti per scopi di screening.

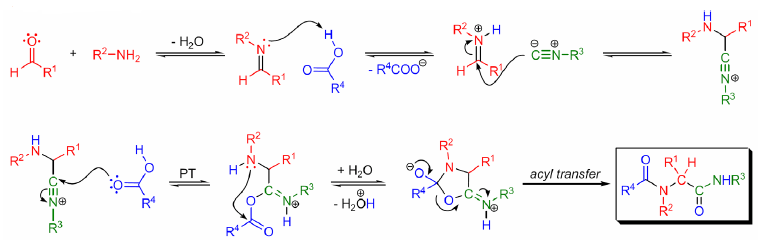
Si ritiene che, meccanicisticamente, si formi prima un'immina dalla condensazione dell'amina con l'aldeide, seguita da addizione dell'ossigeno dell'acido carbossilico e del carbonio dell'immina attraverso il carbonio dell'isonitrile; la risultante isoammide acilata riarrangia tramite transfer di acile generando così il prodotto finale.


Ci sono reazioni del primo e del secondo ordine, e non del terzo ordine!
È una reazione esotermica e spesso termina in secondi o minuti; i solventi polari aprotici sono i migliori, e spesso vengono usati alcoli a basso peso molecolare. La reazione può essere bifasica, e tipicamente si usano concentrazioni dell'ordine di 0.5-2M; in virtù del meccanismo, acidi di Lewis possono accelerare il processo. Preformando la base di Schiff si possono ottenere rese maggiori.
I seguenti utenti ringraziano quimico per questo messaggio: Max Fritz, Mario, Roberto
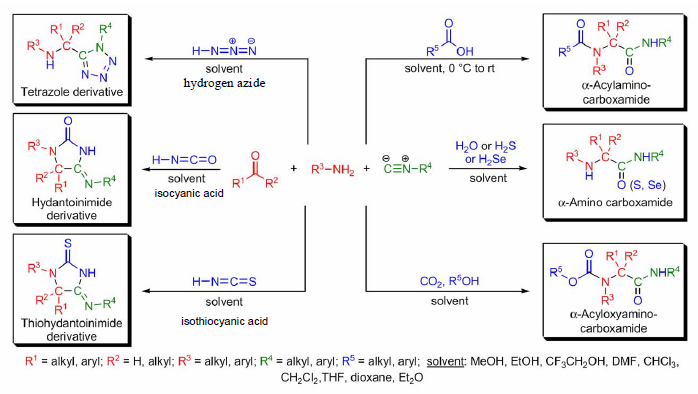
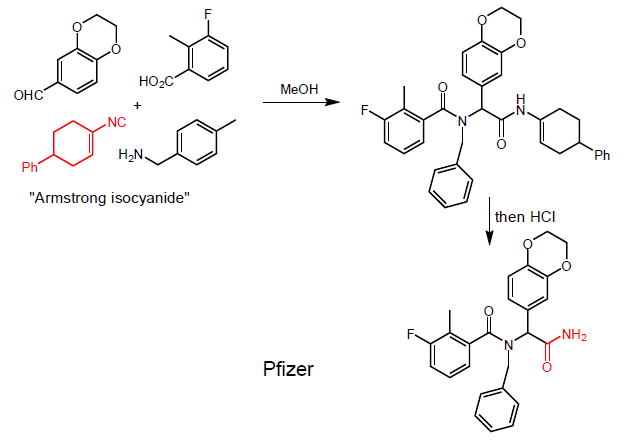
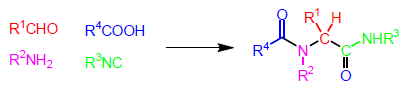 Se in una molecola possono ritrovare una delle parti in colore allora posso esser sicuro che questa è stata sintetizzata tramite Ugi.
Se in una molecola possono ritrovare una delle parti in colore allora posso esser sicuro che questa è stata sintetizzata tramite Ugi.
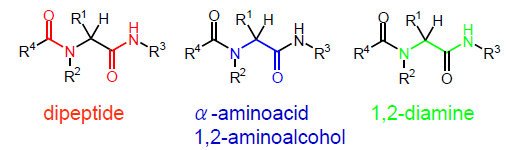 Per quanto concerne il meccanismo, l'isonitrile è sicuramente il componente più interessante.
Per quanto concerne il meccanismo, l'isonitrile è sicuramente il componente più interessante.
 Uno dei meccanismi proposti è questo:
Uno dei meccanismi proposti è questo:
 Di particolare importanza è la versione asimmetrica della reazione di Ugi.
Di particolare importanza è la versione asimmetrica della reazione di Ugi.
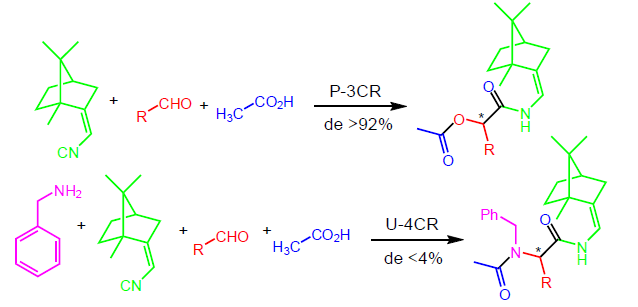
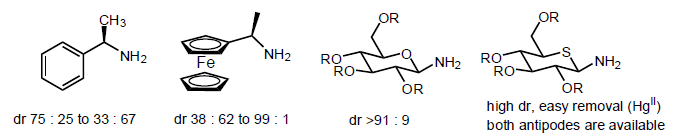
 In principio, ognuno dei quattro componenti, se chirale, può controllare la generazione del nuovo stereocentro.
I risultati migliori sono stati ottenuti con amine chirali, gli altri tre danno bassa o nessuna diastereoselettività.
In generale, la diastereoselettività non è ancora sufficiente.
In principio, ognuno dei quattro componenti, se chirale, può controllare la generazione del nuovo stereocentro.
I risultati migliori sono stati ottenuti con amine chirali, gli altri tre danno bassa o nessuna diastereoselettività.
In generale, la diastereoselettività non è ancora sufficiente.
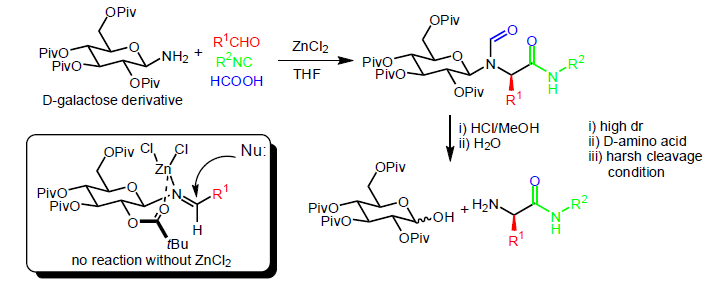 a) Ugi Liebigs Ann. Chem. 1967, 709,11.
b) Ugi J. Am. Chem. Soc. 1970, 92, 1969.
c) Kunz J. Am. Chem. Soc. 1988, 110, 651; Tetrahedron 1988, 44, 6487.
d) Ugi Tetrahedron 2002, 58, 6127.
Ovviamente si possono variare i nucleofili:
a) Ugi Liebigs Ann. Chem. 1967, 709,11.
b) Ugi J. Am. Chem. Soc. 1970, 92, 1969.
c) Kunz J. Am. Chem. Soc. 1988, 110, 651; Tetrahedron 1988, 44, 6487.
d) Ugi Tetrahedron 2002, 58, 6127.
Ovviamente si possono variare i nucleofili:
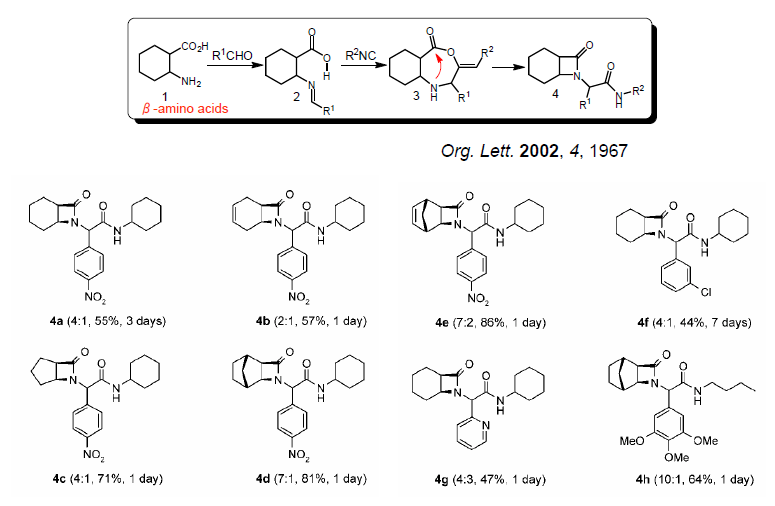
 La reazione può anche essere intramolecolare:
La reazione può anche essere intramolecolare:
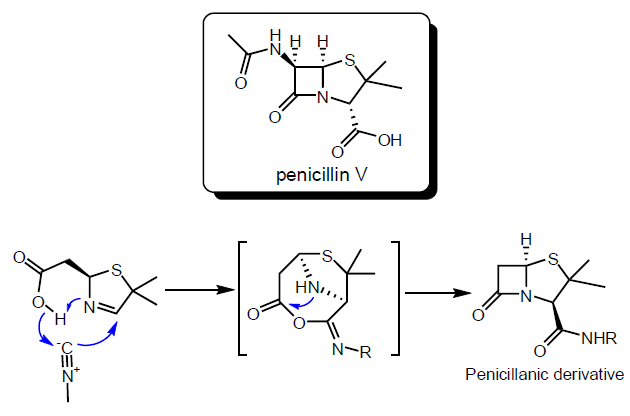 Sintesi di β-lattami:
Sintesi di β-lattami:
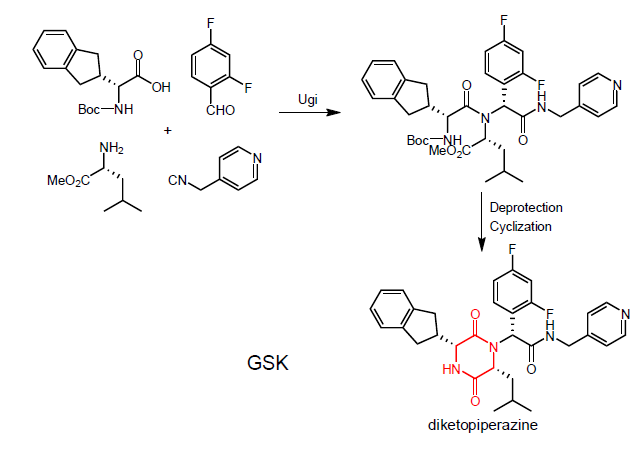
 Sintesi di peptidi ciclici:
Sintesi di peptidi ciclici:
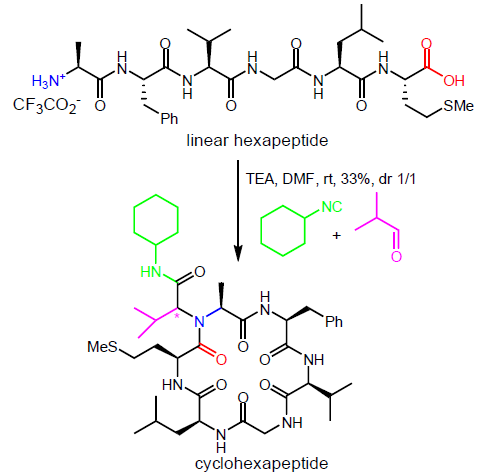 Can. J. Chem. 1979, 57, 32577
Sintesi di 5-aminoossazoli:
Can. J. Chem. 1979, 57, 32577
Sintesi di 5-aminoossazoli:
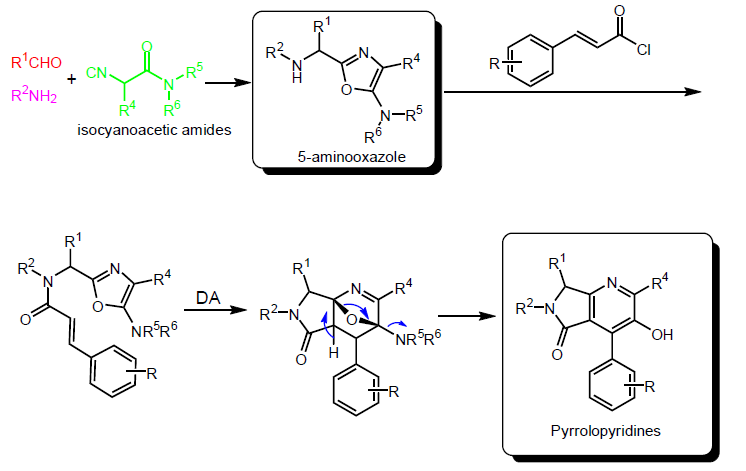
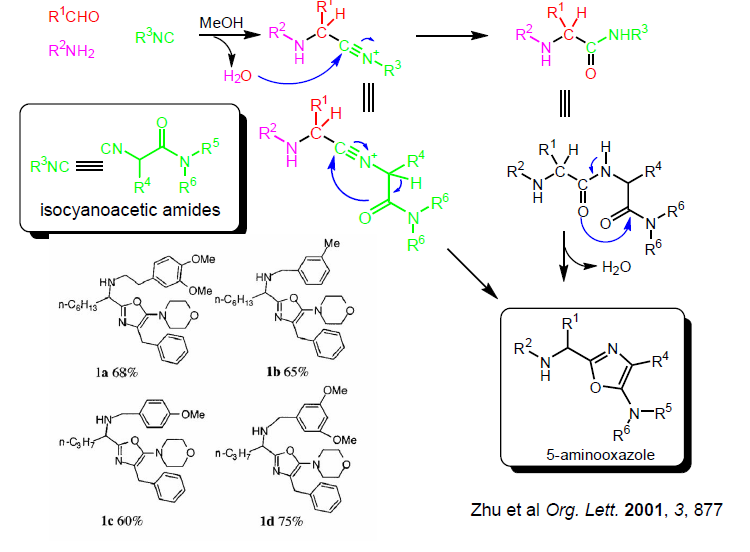 Sintesi di pirrolopiridine:
Sintesi di pirrolopiridine:
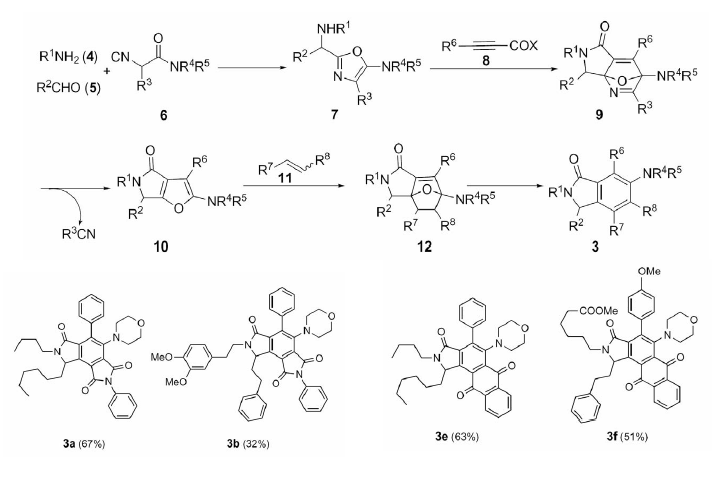
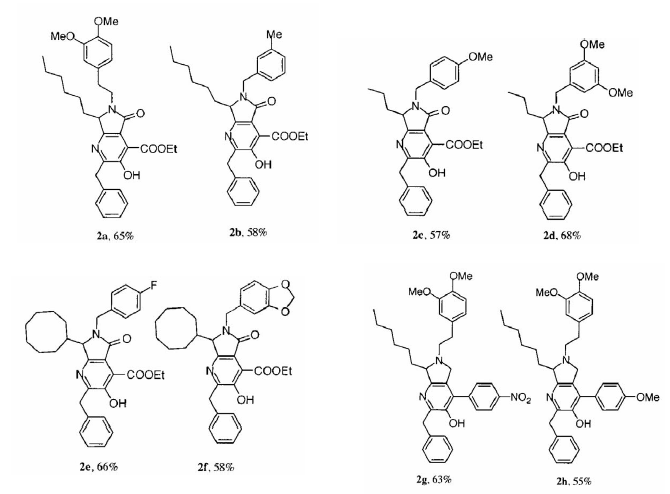 Sintesi di benzeni esasostituiti:
Sintesi di benzeni esasostituiti:
 Tethered Ugi
Tethered Ugi
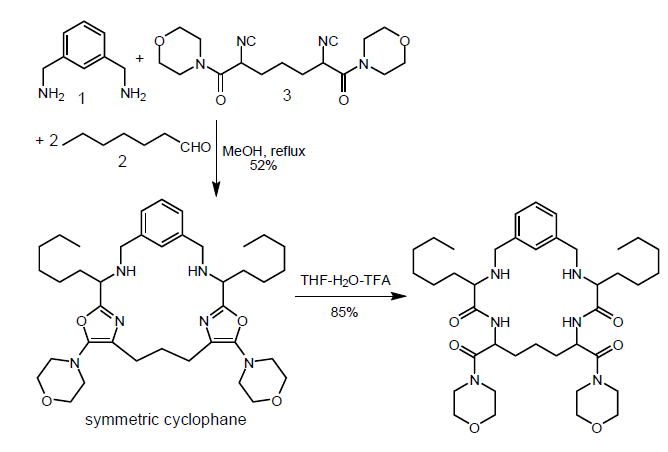 Zhu et al ACIEE 2003, 42, 811
Sintesi di tiazoli
Zhu et al ACIEE 2003, 42, 811
Sintesi di tiazoli
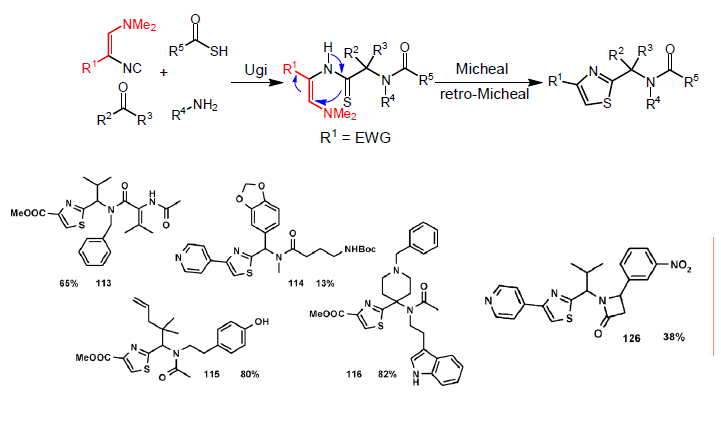 Dömling et al Mol. Diversity 2003, 6, 297; Tetrahedron Letters, 2002, 43, 6897
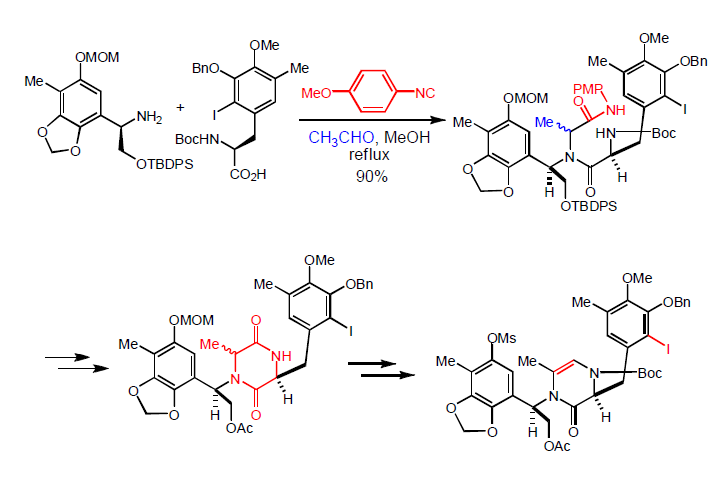
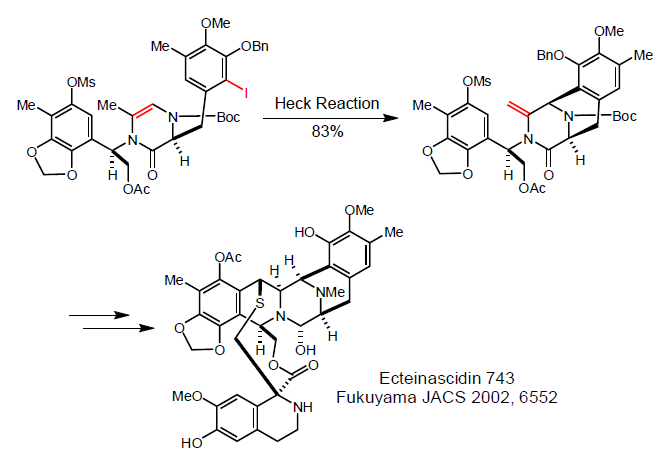
Ugi-Heck o attivazione C-H per sintesi di (iso)chinoline
Dömling et al Mol. Diversity 2003, 6, 297; Tetrahedron Letters, 2002, 43, 6897
Ugi-Heck o attivazione C-H per sintesi di (iso)chinoline
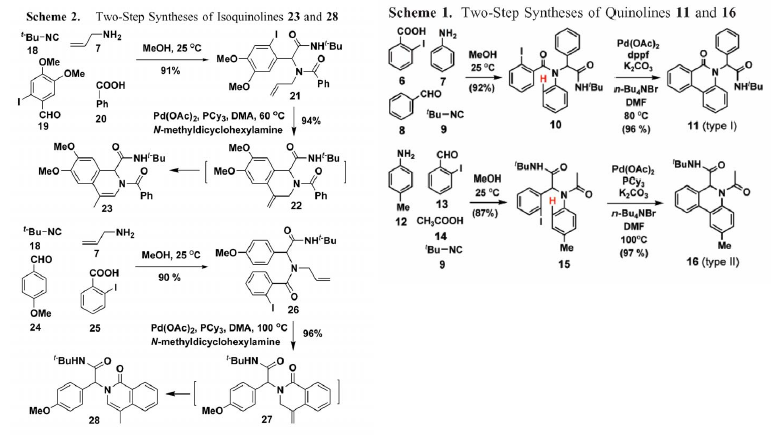 Yang et al J. Comb. Chem. 2006, 8, 696 e 7, 958; Org. Lett. 2004, 6, 3115
Yang et al J. Comb. Chem. 2006, 8, 696 e 7, 958; Org. Lett. 2004, 6, 3115
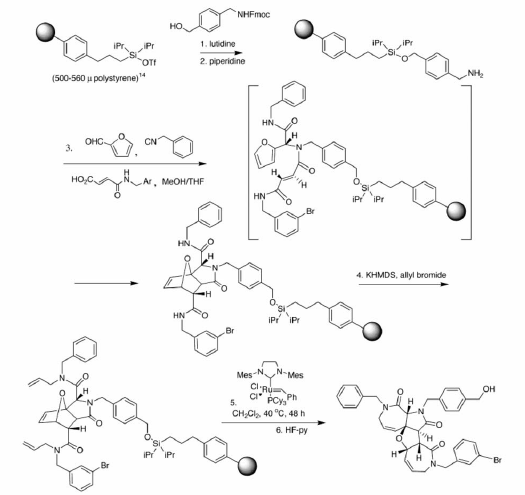 Schreiber et al Org. Lett. 2000, 2, 709 e 2003, 5, 4125
Schreiber et al Org. Lett. 2000, 2, 709 e 2003, 5, 4125
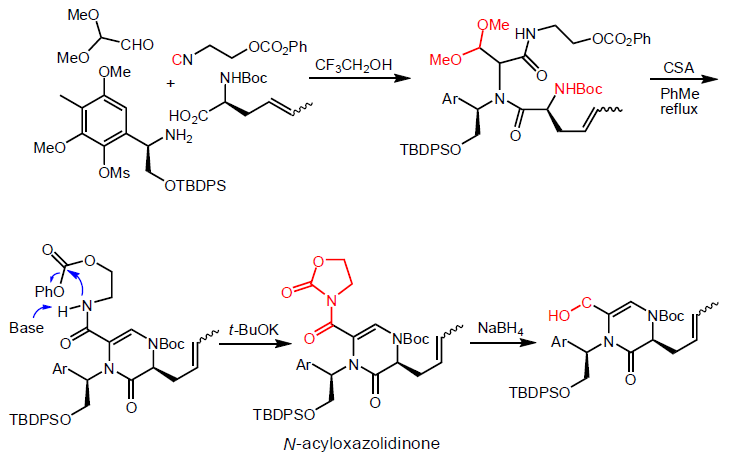
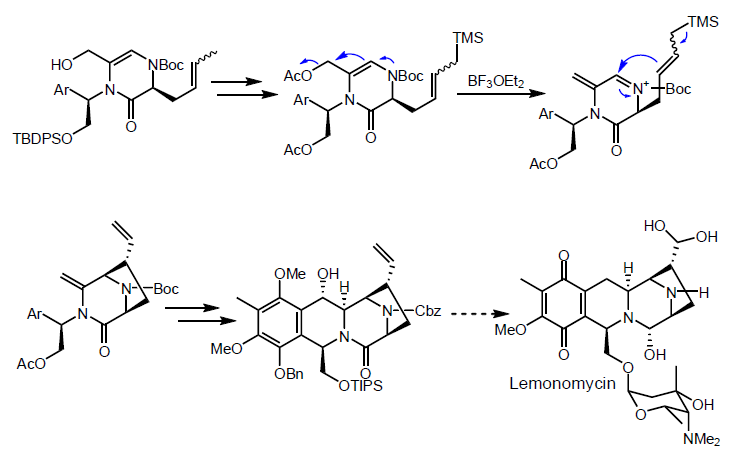
 Se ti fa piacere, inviami pure. A me organica piace tutta.
Anche se i miei campi sono i peptidomimetici, i MOF e i glicosidi, spazio 1po' qua e 1po' là
Se ti fa piacere, inviami pure. A me organica piace tutta.
Anche se i miei campi sono i peptidomimetici, i MOF e i glicosidi, spazio 1po' qua e 1po' là