Mario
2016-05-07 11:37
Si fa ovviamente riferimento al Sandmeyer e alla sua innovativa, per allora (Sandmeyer, T. Ber. Dtsch. Chem. Ges. 1884, 17, 2650–2653, Ueber die Ersetzung der Amid-gruppe durch Chlor, Brom und Cyan in den aromatischen Substanzen.) modalità di introduzione di alogeni in un anello aromatico mediante sali di diazonio intermedi.
Niente di meglio che ricordarlo ripetendo la sua esperienza in un classica sintesi, con i reagenti di un tempo e scegliendo un composto di partenza non proprio banale. Per la sua semplicità la Sandmeyer è ancora oggi una valida via per preparare composti altrimenti difficili da sintetizzare, oltretutto con mezzi molto alla portata di un homelab.
Ho perciò optato come sintesi quella dell'acido 2-bromobenzoico.
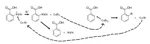
Il meccanismo di reazione è qui sotto illustrato
La reazione avviene tramite un meccanismo di trasferimento di carica (single electron transfer) da parte dell’alogenuro rameoso. Si forma così bromuro rameico e il radicale diazo che si decompone liberando azoto gassoso e un radicale arilico. Questi reagisce con il bromuro rameico rigenerando l’iniziale bromuro rameoso e contemporaneamente si forma il 2-bromoderivato.
Sintesi
In un beker da 50 ml si introducono nell’ordine: 1,75 g di solfato di rame pentaidrato, 5,0 g di NaBr, 15 ml di acqua, 1,5 g di truciolini di rame (più fini sono meglio è) e 1,65 g di acido solforico conc. Si porta il tutto ad ebollizione coprendo il beker con un vetro d'orologio. La soluzione diventa rapidamente di colore bruno scuro e dopo un po inizia a formarsi un precipitato di bianco di Cu2Br2 . Proseguire l’ebollizione fino ad avere lo scoloramento del liquido.
La velocità con cui questo avviene dipende dallo stato di suddivisione del rame. Con Cu in trucioli finissimi ciò accade in relativamente poco tempo.
Aggiungere allora 2 g di acido antranilico, mescolare bene e fare raffreddare a circa 5 °C.
A parte preparare una soluzione con NaNO2 (1,1g + 5 ml di acqua). Aggiungere questa soluzione goccia a goccia alla precedente. Durante questa fase non bisogna superare i 10 °C, quindi occorre mantenere il beker immerso in un bagno di acqua +ghiaccio. Agitare in continuazione con un termometro. Nel punto dove cade la goccia si noterà l’apparire di un colore verde (dovuto all'alogenuro rameico) che subito scompare agitando (si riforma il bromuro rameoso bianco). Si forma anche molta schiuma (per lo svolgimento di azoto gassoso). La fine reazione si capisce dal comparire della colorazione verdastra stabile ( la quale si forma per ossidazione a Cu++ da parte del nitrito in eccesso).
Lasciare quindi riposare il contenuto a temperatura ambiente per alcune ore agitando ogni tanto.
Si filtra lavando con acido solforico 1M e poi con acqua fredda.
Si ottengono 3,3 g del prodotto grezzo

Per ottenere un prodotto più puro ed esente per quanto possibile da sali di rame di effettua una doppia cristallizzazione con 100 ml di HCl 0,1M bollente. In questo modo si perde alquanto prodotto ma si guadagna in purezza. ecco il risultato finale:
saluti
Mario
I seguenti utenti ringraziano Mario per questo messaggio: luigi_67, Beefcotto87, zodd01, fosgene, Roberto, LuiCap, Hamiltoniano, ohilà, quimico, ClaudioG., thenicktm