zodd01
2023-02-14 13:45
Buongiorno a tutti,
oggi vi porto un'altra bella sintesi e per di piú in scala pilota: la preparazione del benzene da plastica riciclata. La reazione utilizzata é la pirolisi, cioé il riscaldamento diretto ad alta temperature in assenza/carenza di ossigeno, conosciuta pure come distillazione secca. In rete, su YT ci sono tanti video sul benzene da acido benzoico, acido tereftalico, ma noi invece trasformiamo direttamente un rifiuto, bottiglie di PET, in una risorsa. E' un esempio di riciclo chimico, di economia circolare.
Reazione e setup
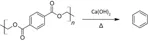
In questa pirolisi il PET viene fatto reagire con calce spenta, la quale in complessivo, fa da catalizzatore. Come proposto dal riferimento, la calce idrolizza il PET, liberando il glicole e formando calcio tereftalato, il quale poi decarbossila a benzene e calcio carbonato. Il carbonato a sua volta con l'alta temperatura si decarbossila a CaO e anidride carbonica. Il ciclo riparte ma c'é da puntualizzare man mano che la calce si disidrata, dopo ripetute pirolisi, ho constatato l'idrolisi avviene sempre piú difficilmente. Il riferimento stesso menziona il fatto di utilizzare calce spenta invece che viva aiuta l'idrolisi del PET per via dell'acqua liberata durante la reazione.
Come pirolizzatore ho riadattato un articolo venduto come distillatore su eBay, al prezzo di circa 100 euro. E' un bel recipiente di acciaio, 11.4 litri, a chiusura ermetica, termometro incluso e refrigerante a spirale. Svolge bene il proprio lavoro. Il pirolizzatore é posto su un fornello alimentato a gas e coperto ai lati con mattonelle di ceramica. La coda del refrigerante é inserita dentro una beuta da vuoto da 500 ml, coperta alla meglio con del foglio di alluminio.


Si tagliano 500 g di bottiglie di plastica in piccoli pezzetti, scartando tappo ( non é PET ), etichetta, testa e fondo. A parte si pesano 1.5 kg di calce idrata ( spenta ), si mescolano intimamente dentro la caldaia. La proporzione é quindi 3:1 calce : PET. Chiusa la caldaia e accesa la pompa dell'acqua, si avvia il riscaldamento, tenendo la fiamma inizialmente bassa. Dei fumi appaiono presto dentro la beuta di raccolta. Dopo pochi minuti la fiamma viene aumentata al massimo, la quale porta velocemente i gas di pirolizzato oltre i 200 Celsius. Il pirolizzato inizia ad uscire giallo - verdognolo, insieme ad acqua ed una fase insolubile, le cere. Un sottoprodotto dato da pirolisi incompleta, fastidiosissimo e problematico. Dopo 2 ore, si interrompe il riscaldamento e si lascia tutto raffreddare naturalmente. Si recupera il pirolizzato dalla beuta di raccolta, si separa lo strato acquoso insieme a piú cera possibile cautamente per non perdere prodotto. La fase organica si estrae con 3 x 50 ml di acqua e poi si filtra e rifiltra pazientemente per gravitá la fase organica su cotone fino a quando non rimangono piú residui cerosi. Richiede giorni e notti.
Il pirolizzato, da giallo verdognolo imbrunisce presto all'aria. In questo particolare batch si sono ottenuti 45 g ( 47 ml ) di prodotto corrispondente al 9% della massa iniziale di PET. E' caratterizzato tramite indice di rifrazione e densitá. Il primo é fuori scala di un rifrattometro 80 Brix, cioé maggiore di n20 = 1.49701. Nella caldaia rimangono insieme alla calce residui carboniosi.
Discussione
Il riferimento ha studiato varie proporzioni di calce : PET, e noi pure abbiamo seguito le loro indicazioni. Riguardo temperature e tempo di reazione, 300 Celsius e 2 h garantiscono una reazione piú completa: tutte le prove sono state eseguite in queste condizioni. La resa del batch descritto é bassissima se pensiamo l'articolo, dichiara 43.7% di frazione liquida per quella proporzione. Dai gas cromatogrammi, gli autori descrivono un pirolizzato costituito in maggioranza da benzene ma anche toluene, stirene, acido benzoico, acetofenone, indene, naftalene, bifenile. All'aumentare del rapporto calce : PET, i componenti solidi del pirolizzato diminuiscono ad iniziare dal 5:1, la reazione essere sempre piú selettiva verso il benzene. Nelle varie prove eseguite, dalla densitá, resa e apparenza del pirolizzato si confermano le stesse conclusioni degli autori. Il rapporto 5:1 conferisce un prodotto piú pulito e una resa superiore al 3:1. Il 4:1 dá una resa ancora piú alta ma dovuta a un prodotto piú contaminato da cere ( densitá del benzene 0.876 g/ml ). La calce si puó riciclare ma il prodotto diventa sempre piú sporco e la resa molto variabile. I pirolizzati lasciati decantare per settimane rilasciano ancora un sedimento ceroso. Infine dei semplici test di infiammabilitá sono realizzati con diversi pirolizzati.
La migliore opzione é quindi usare rapporti calce : PET e possibilmente calce nuova, o almeno lasciata a reidratare all'aria.
Purificazione
Accumulato abbastanza materiale, si procede alla distillazione. Circa 250 ml di pirolizzato, da diversi batch, sono introdotti un pallone da 500 ml, messi in bagno d'olio a 100 Celsius e distillati semplici. La frazione che passa al di sotto 75 Celsius é scartata ( 20 ml circa ), mentre quella fra 78 - 80 Celsius recuperata. Si ottengono all'incirca 95 ml di distillato limpido e leggermente giallino. Ció che rimane é la frazione piú pesante di toluene, xileni, etilbenzeni e composti aromatici solidi vari.
p. eb.: 79 - 80 Celsius
d20 = 0.870 g/ml
Riferimenti
1. Chem. Lett. vol. 33, pp. 282-283, 2004
I seguenti utenti ringraziano zodd01 per questo messaggio: fosgene, Mercaptano, ChemLore, luigi_67, Teor.Ema, Copper-65, ale93