EdoB
2021-06-20 19:38
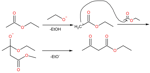
L'acetoacetato di etile è un β-chetoestere molto utile in sintesi organica. In laboratorio può essere prodotto attraverso una condensazione di Claisen. Il meccanismo non è molto complesso. Il carbonio in alfa di una molecola di acetato di etile viene deprotonato dall'etilato di sodio. Il carbanione che si forma attacca il carbonio carbonilico di un'altra molecola di estere facendo aprire il doppio legame C=O. Nell'ultimo passaggio, viene spontaneamente eliminata una molecola di CH3CH2O(-), ovvero il catalizzatore basico.
Il catalizzatore basico viene prodotto in situ per reazione del sodio metallico con le tracce di etanolo presenti nell'acetato di etile tecnico. Anche le tracce di acqua portano alla formazione di etilato di sodio:
2H2O + 2Na --> H2 +2NaOH
NaOH + AcOEt--> AcONa + EtOH
2EtOH + 2Na --> H2 + EtONa
Questa serie di reazioni, anche se portano alla formazione di etilato di sodio, comportano un uso maggiore di sodio. Si può dire pertanto che l'estere di partenza non deve essere anidro nel senso stretto del termine, ma bisogna tenere conto del fatto che l'acqua eventualmente presente porterà a rese minori.
Reagenti
- Acetato di etile
- Sodio metallico
- Acido acetico
- Cloruro di sodio
- Soluzione satura di cloruro di sodio
Procedimento
In un pallone da 1L vengono messi 250g di acetato di etile e 25 g di sodio, tagliato in pezzi piccoli. Montato un refrigerante, si agita magneticamente. Lahttps://drive.google.com/file/d/1SbDIUezGAmayQ6PiKAHRhTyIdgG4tCN2/view?usp=sharing reazione inizia dopo un breve periodo di latenza, che dipende dal contenuto in acqua ed alcol nel solvente. La reazione è esotermica ma non tende a sfuggire di mano, dato il grande eccesso di solvente. Dopo un paio di ore, tutto il sodio ha reagito e non ve ne è più traccia nel pallone. Se gli ultimi pezzetti fanno fatica a reagire, è possibile scaldare. La https://drive.google.com/file/d/126DMOXw9jUHTfJDa-yiTUU-nWC1avDhz/view?usp=sharingmiscela di reazione, trascorso il tempo, è limpida, rosso-arancio, e presenta una debole fluorescenza verde ai raggi UV. La soluzione viene lasciata raffreddare e poi si aggiungono cautamente, monitorando la temperatura, 140 mL di acido acetico al 50%. Inizialmente si forma un precipitato che rende difficoltosa l'agitazione. Continuando con le aggiunte di acido, e mescolando manualmente, il solido si ridiscioglie. Si satura la soluzione con NaCl. Le due fasi che si formano vengono separate e, quella superiore, viene lavata con una soluzione satura di NaCl per allontanare buona parte dell'acqua disciolta. La fase organica viene sottoposta a distillazione. La prima frazione che distilla è etilacetato in eccesso, che può essere recuperato. Una volta rimosso tutto il solvente, si procede distillando a pressione ridotta il prodotto (76-80°C/18mm). Tutte e 2 le volte che ho ripetuto questa sintesi ho ottenuto https://drive.google.com/file/d/1UGTp5IcS2T997VaBIYQCDEeEkDVOGKwh/view?usp=sharing2 frazioni di purezze diverse, una prima perfettamente limpida e una seconda giallo chiaro, leggermente fluorescente agli UV. Ho deciso di conservare la seconda frazione tal quale, la purificherò quando mi servirà. La resa di estere "incolore" è di circa 46 g (24,5%). Se aggiungiamo anche i 15,38 g di estere leggermente colorato la resa sale al 33%. La procedura di http://www.orgsyn.org/demo.aspx?prep=CV1P0235OrgSyn riporta rese del 28-29%.
Reagenti


Reazione
Prodotto
Meccanismo di reazione
I seguenti utenti ringraziano EdoB per questo messaggio: myttex, Geber, Copper-65