EdoB
2022-12-23 08:55
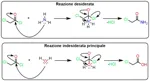
La 2-cloroacetammide è una molecola organica molto semplice che trova uso come reagente nella sintesi di numerosi composti di interesse farmaceutico. Esistono diverse sintesi di questo composto, io ho deciso di far reagire il cloruro di cloroacetile con ammoniaca acquosa.
Reagenti
- Ammoniaca 30%
![[Corrosivo]](images/corrosivo.png.pagespeed.ce.CTVEf8LXM3.png)
![[Pericoloso per l'ambiente]](images/ambiente.png.pagespeed.ce.MDbzeDsUFv.png)
![[Irritante]](images/irritante.png)
- cloruro di cloroacetile
![[Pericoloso per l'ambiente]](images/ambiente.png.pagespeed.ce.MDbzeDsUFv.png)
![[Perocoloso per la salute]](images/salute.png)
![[Tossico]](images/tossico.png)
![[Corrosivo]](images/corrosivo.png.pagespeed.ce.CTVEf8LXM3.png)
- etere etilico
![[Infiammabile]](images/infiammabile.png)
![[Irritante]](images/irritante.png)
- metanolo gelato (-20°C)
![[Infiammabile]](images/infiammabile.png)
![[Tossico]](images/tossico.png)
![[Perocoloso per la salute]](images/salute.png)

Procedimento
In una beuta da 50 mL vengono introdotti 10mL di ammoniaca concentrata. Dopo aver raffreddato esternamente la beuta con acqua e ghiaccio, si gocciolano lentamente 5mL di cloruro di cloroacetile che reagisce violentemente con l'ammoniaca liberando un denso fumo bianco che non va assolutamente inalato. Terminata l'aggiunta, si controlla il pH che dovrebbe essere lievemente acido, nel caso in cui non lo fosse, è utile portarlo a pH 5-6 aggiungendo ammoniaca o acido acetico. Se l'ammoniaca è presente in largo eccesso, con il calore della reazione, potrebbe formarsi della 2-amminoacetammide oltre che al prodotto desiderato. Per evitare questo fenomeno il più possibile, è importante avere un leggero eccesso di ammoniaca così da favorire la reazione del cloruro acilico con NH3 e sfavorire quella con H2O senza però esagerare. In ogni caso, i sottoprodotti sono molto più solubili in acqua del prodotto principale quindi la purificazione è agevolata.
Terminata l'aggiunta, la sospensione di cristalli ottenuta viene raffreddata e 0°C e poi filtrata su setto poroso. La beuta e il solido vengono lavati con metanolo gelato e poi etere etilico. Quando il prodotto è apparentemente asciutto, viene seccato ulteriormente a 80°C. La resa è di 3,056 g (51%)
I seguenti utenti ringraziano EdoB per questo messaggio: luigi_67, FLaCaTa100, LuiCap, Mercaptano, fosgene, ChemLore, Copper-65, Claudio, zodd01