quimico
2011-11-18 10:34
Mi piacerebbe inagurare una serie, piccola, di sintesi totali di molecole naturali a scheletro molto complesso. So bene che forse per i più sono cose noiose, molto complesse e che non si capisce molto ma ci tenevo a far vedere che la sintesi organica non serve solo a giocare con la chimica ma anche ad esplorare la Natura, cercando di imparare da essa e a volte spingere l'uomo a copiare da essa. Non è facile né tantomeno istantaneo a volte cercare di replicare. Qui si tratta di sintesi che sono costate anche anni di sintesi, tentativi senza successo. Ma a mio parare è bello riuscire ad arrivare fino in fondo. Specie se poi tali molecole possono salvare vite umane, ed evitare che organismi viventi come noi vengano uccisi. Inutilmente. Perché spesso per 1mg di sostanza sono richiesti anche più di 100kg di piante, organismi marini, o animali.
Questa è una delle diverse sintesi totali di questa molecola. In particolare è stata fatta da Ian Paterson, Gordon J. Florence, Kai Gerlach, Jeremy P. Scott, e Natascha Sereinig (Contribution from the UniVersity Chemical Laboratory, Cambridge UniVersity, Lensfield Road, Cambridge CB2 1EW, UK) ed è stata pubblicata sul J. Am. Chem. Soc. 2001, 123, 9535-9544.
La discodermolide (1) è un unico polichetide isolato da Gunasekera e collaboratori all'Harbor Branch Oceanographic Institute nel 1990 dalla spugna che vive nelle profondità del Mar dei Caraibi Discodermia dissoluta1,2. La sua struttura grossolana fu determinata tramite approfonditi studi spettroscopici e la sua stereochimica relativa fu assegnata tramite cristallografia a raggi X di cristallo singolo.
Strutturalmente, essa ha 13 centri stereogenici, un δ-lattone tetrasostituito (C1-C5), un doppio legame disostituito ed un doppio legame trisostituito (Z), un pendente recante una funzionalità carbammato (C19), ed uno (Z)-diene terminale (C21-C24).
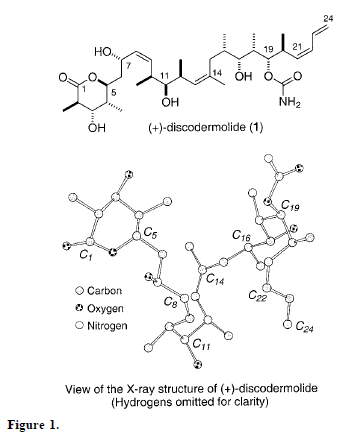
Allo stato solido, la discodermolide adotta la conformazione a forma di U mostrata in Fig. 1, dove le due olefine (Z) interne nella catena laterale agiscono da bloccanti della conformazione tramite minimizzazione della tensione A(1,3) tra i loro rispettivi sostituenti assieme all'evitare interazioni syn-pentano, mentre il δ-lattone tetrasostituito preferisce una conformazione tipo-barca.
Il polichetide con uno scheletro carbonico a 24 membri della discodermolide
sembra essere costituito da otto unità propionato e quattro unità acetato.
È probabile che questo dodecachetide sia sintetizzato da un microorganismo simbiotico associato alla specie Discodermia dissoluta, che coinvolge una sintasi polichetidica modurale.
La discodermolide inizialmente fu riscontrato essere un potente agente immunosoppressore, sia in vivo che in vitro, oltre a mostrare un'attività antifungina3. Essa inibiva la proliferazione di cellule T con un IC50 di 9 nM ed un problema di rigetto in sorci trapiantati.
Successivi screening biologici di questo composto rivelarono una citotossicità sorprendente, che causava un arresto del ciclo cellulare nella fase G2/M in una varietà di linee cellulari umane e di topi4.
La discodermolide fa parte del gruppo di agenti antimicotici mostrati in Fig. 2 ora noti per l'agire tramite stabilizzazione di microtubuli inclusi il Tassolo(2)5a, gli epotiloni A e B (3, 4)5b, l'eleuterobina (5)5c e più recentemente, la laulimalide (6)5d.
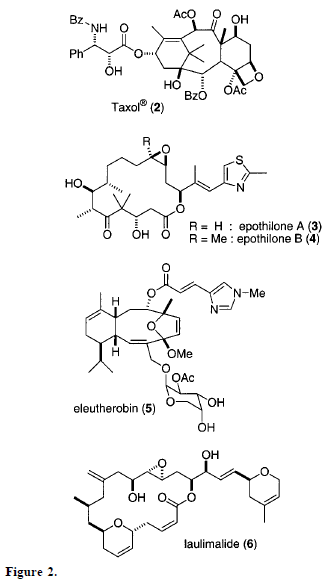
La discodermolide è stata riconosciuta come uno dei più potenti agenti di polimerizzazione di tubuline noti al giorno d'oggi. Nonostante non possieda apparenti simili strutturali, la discodermolide è stato riscontrato stabilizzare i microtubuli in modo più potente del Tassolo (2, paclitaxel) ed inibisce competitivamente il suo legarsi a polimeri tubulinici4,6.
La crescita di cellule cancerose nelle ovarie e nel colon resistenti al Taxolo viene inibita dalla discodermolide con un IC50 di < 2.5nM7 mentre la regolazione e il tipo di frammentazione del DNA indotto è consistente con l'induzione di apoptosi8.
In recenti studi comparativi della discodermolide, gli epotiloni e l'eleuterobina rispetto ad una linea cellulare del carcinoma umano ai polmoni Tassolo-dipendente (A549-T12)9, è stata trovato che la discodermolide era incapace di agire da sostituto del Tassolo, mentre gli epotiloni e l'eleuterobina erano in grado di mantenere la vitalità della linea cellulare. In modo significativo, la presenza di basse concentrazioni di Tassolo amplificava la citotossicità della discodermolide di 20 volte
rispetto a questa linea cellulare. Comunque, questo effetto sinergico in vitro non è stato osservato con combinazioni di epotiloni o
eleuterobina con il Tassolo.
Il profilo biologico più incoraggiante della discodermolide (1) la rende un promettente candidato per lo sviluppo clinico quale agente chemioterapico per i tumori alla mammella, alle ovaie, e al colon Tassolo-resistenti e per altri tumori resistenti a più farmaci.
Lo sviluppo clinico, tuttavia, è gravemente ostacolato dall'estramamente scarsa scorta di discodermolide (0.002% p/p spugna congelata) derivata dalla fonte naturale (una rara spugna che si trova in fondali profondi e che si trova solo nei Caraibi e che richiede l'uso di sommergibili con equipaggio per la sua raccolta).
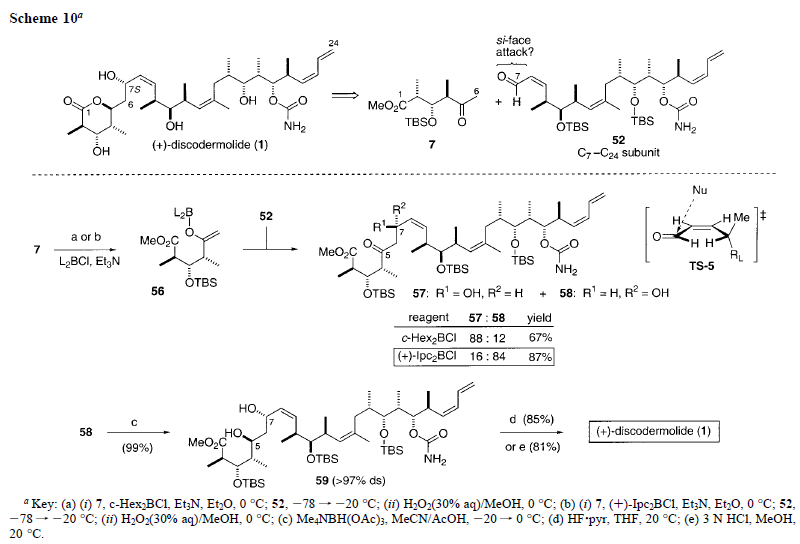
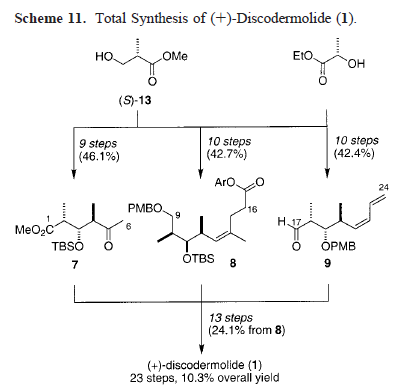
Perciò, la sintesi totale al giorno d'oggi costituisce l'unica via percorribile per le quantità utili di questi nuovo polichetide citotossico. Di conseguenza, ci sono stati considerevoli sforzi sintetici nei confronti della discodermolide, che sono culminati in diverse sintesi totali10 e numerose sintesi di frammenti11. Infatti, la configurazione assoluta della discodermolide fu stabilita da Schreiber e collaboratori tramite la loro sintesi iniziale sia della (+)- che della (-)-discodermolide10a,b. Qui, sono riportati i dettagli completi dello svilluppo di una nuova sintesi totale, basata su aldoli12a della (+)-discodermolide per fornire quantità utili di questo importante prodotto marino naturale, con sintesi migliorate di frammenti e coupling, ed alcuni nuovi analoghi strutturali12b. Specialmente, la sintesi ottimizzata dagli autori implica una strategia davvero efficace di coupling dei frammenti, distinta da tutti gli approcci precedentemente riportati, che porta ad una resa totale del 10.3% (su 23 passaggi lineari) ed offre il potenziale per la produzione di quantità considerevoli di (+)-discodermolide, aiutando quindi a ridurre il problema delle scorte e permettendo il suo successivo sviluppo nella chemioterapia contro i tumori.
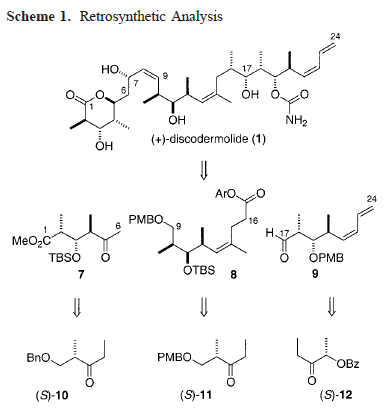
 Sintesi della subunità C9-C16, 8. Uno degli aspetti più sinteticamente impegnativi della discodermolide è l'introduzione efficiente della (Z)-olefina trisostituita C13-C14.
Le precedenti sintesi avevano adottato metodi convenzionali per la sua costruzione, cioè olefinazioni di Wittig, ma queste si erano spesso dimostrate inaffidabili, esibendo rese e selettività variabili10c,g.
Il loro frammento C9-C16 8 richiedeva una funzionalità carbonile attaccata al C16 per permettere il coupling del frammento basato sull'aldolica. L'elegante metodologia di espansione d'anello tipo Claisen, sviluppata in modo accurato da Holmes e collaboratori per la sintesi di lattoni di medie dimensioni, permette simultaneamente l'installazione di questa funzionalità e della (Z)-olefina trisostituita C13-C1422.
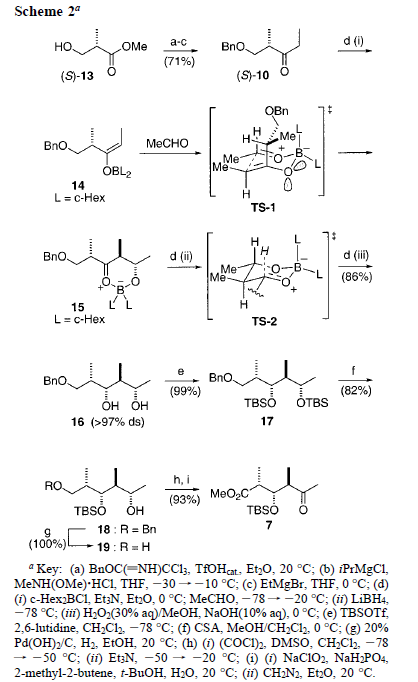
La sintesi del frammento aril estere C9-C16 8 iniziava dal chetone protetto con PMB (S)-11 (Schema 3)15. Questo era ottenuto in tre passaggi (77% resa totale, 0.2 mol scala) dal
metil (S)-3-idrossi-2-metilpropionato, (S)-13, in condizioni simili a quelle descritte sopra per il chetone benzil protetto (S)-10. Nelle loro condizioni standard (c-Hex)2BCl/Et3N14, l'enolizzazione (E) del chetone (S)-11, e la reazione con la metacroleina ha portato, dopo workup ossidativo, all'antialdolo prodotto previsto 20 (95%, >97% ds)23. La riduzione 1,3-anti controllata dal substrato del β-idrossi chetone è stata ottenuta nelle condizioni di Evans-Tischenko24 con SmI2 e propionaldeide,
a dare l'1,3-diolo monoestere 21 (96%, >97% ds). La metanolisi (K2CO3, MeOH) fornisce quindi il previsto diolo 1,3-anti 22 (97%).
Alternativamente, la riduzione del β-idrossi chetone 20 è stata condotta usando Me4NBH(OAc)3 in MeCN e AcOH a dare direttamente il diolo 1,3-anti 22 (94%, >97% ds). Mentre l'ultimo metodo accorcia la via sintetica, c'era un po' di meno riconducibile al rendimento materiale rispetto alla procedura in due passaggi.
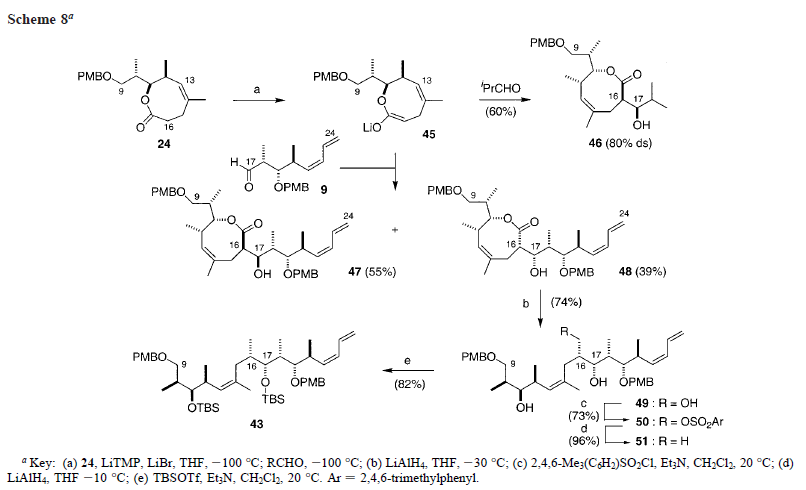
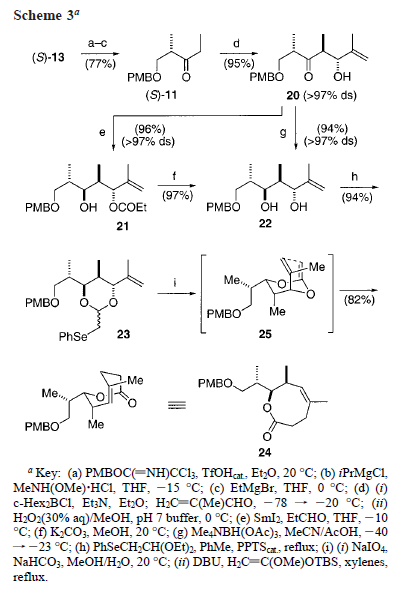
Seguendo il protocollo di Holmes22e il fenilselenoacetale 23 era stato ottenuto tramite scambio di acetale del 2-fenilselenoacetaldeide dietilacetale col diolo 22 in condizioni acide. Questo fornisce il precursore di Claisen aspettato 23 come miscela diastereoisomerica irrilevante 2:1 al carbonio acetalico (94%). L'ossidazione della selenide 23 a selenossido è stata facilmente ottenuta con NaIO4. Il prodotto grezzo è stato quindi direttamente sottoposto alle condizioni del riarrangiamento di Claisen forendo il desiderato lattone ad otto membri 24 con una resa dell'82%, assieme alla recuperata selenide 23 (18%), che può essere riciclata. La formazione esclusiva della (Z)-olefina trisostituita C13-C14 può essere attribuita alla preferita conformazione biciclica a sedia adottata dal chetene acetale 25, come mostrato nello Schema 3. Queste condizioni erano riconducibili alla produzione di quantità multigrammo del lattone ad otto membri 24.
Sintesi della subunità C9-C16, 8. Uno degli aspetti più sinteticamente impegnativi della discodermolide è l'introduzione efficiente della (Z)-olefina trisostituita C13-C14.
Le precedenti sintesi avevano adottato metodi convenzionali per la sua costruzione, cioè olefinazioni di Wittig, ma queste si erano spesso dimostrate inaffidabili, esibendo rese e selettività variabili10c,g.
Il loro frammento C9-C16 8 richiedeva una funzionalità carbonile attaccata al C16 per permettere il coupling del frammento basato sull'aldolica. L'elegante metodologia di espansione d'anello tipo Claisen, sviluppata in modo accurato da Holmes e collaboratori per la sintesi di lattoni di medie dimensioni, permette simultaneamente l'installazione di questa funzionalità e della (Z)-olefina trisostituita C13-C1422.
La sintesi del frammento aril estere C9-C16 8 iniziava dal chetone protetto con PMB (S)-11 (Schema 3)15. Questo era ottenuto in tre passaggi (77% resa totale, 0.2 mol scala) dal
metil (S)-3-idrossi-2-metilpropionato, (S)-13, in condizioni simili a quelle descritte sopra per il chetone benzil protetto (S)-10. Nelle loro condizioni standard (c-Hex)2BCl/Et3N14, l'enolizzazione (E) del chetone (S)-11, e la reazione con la metacroleina ha portato, dopo workup ossidativo, all'antialdolo prodotto previsto 20 (95%, >97% ds)23. La riduzione 1,3-anti controllata dal substrato del β-idrossi chetone è stata ottenuta nelle condizioni di Evans-Tischenko24 con SmI2 e propionaldeide,
a dare l'1,3-diolo monoestere 21 (96%, >97% ds). La metanolisi (K2CO3, MeOH) fornisce quindi il previsto diolo 1,3-anti 22 (97%).
Alternativamente, la riduzione del β-idrossi chetone 20 è stata condotta usando Me4NBH(OAc)3 in MeCN e AcOH a dare direttamente il diolo 1,3-anti 22 (94%, >97% ds). Mentre l'ultimo metodo accorcia la via sintetica, c'era un po' di meno riconducibile al rendimento materiale rispetto alla procedura in due passaggi.
Seguendo il protocollo di Holmes22e il fenilselenoacetale 23 era stato ottenuto tramite scambio di acetale del 2-fenilselenoacetaldeide dietilacetale col diolo 22 in condizioni acide. Questo fornisce il precursore di Claisen aspettato 23 come miscela diastereoisomerica irrilevante 2:1 al carbonio acetalico (94%). L'ossidazione della selenide 23 a selenossido è stata facilmente ottenuta con NaIO4. Il prodotto grezzo è stato quindi direttamente sottoposto alle condizioni del riarrangiamento di Claisen forendo il desiderato lattone ad otto membri 24 con una resa dell'82%, assieme alla recuperata selenide 23 (18%), che può essere riciclata. La formazione esclusiva della (Z)-olefina trisostituita C13-C14 può essere attribuita alla preferita conformazione biciclica a sedia adottata dal chetene acetale 25, come mostrato nello Schema 3. Queste condizioni erano riconducibili alla produzione di quantità multigrammo del lattone ad otto membri 24.
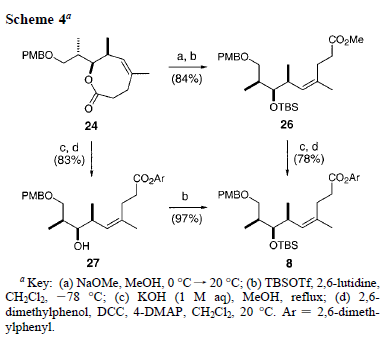
 La conversione del lattone 24 ad aril estere 8 era ora richiesta (Schema 4). Inizialmente, è stata impiegata una sequenza di quattro passaggi, in base a cui la metanolosi del 24 e la protezione come TBS del risultante idrossi estere ha fornito il 26 (84%, 2 passaggi), e la saponificazione e l'esterificazione con 2,6-dimetilfenolo nelle condizioni di Steglich25 ha fornito il frammento chiave 8 (78%, 2 passaggi).
Successivamente, una più corta sequenza di tre passaggi è stata impiegata per ottenere il frammento chiave 8 con una resa totale dell'81%. Questa comportava la diretta apertura del lattone 24 ad idrossi acido intermedio ed esterificazione25 con 2,6-dimetilfenolo a dare l'idrossi estere 27, seguita da protezione come TBS a dare 8. Riassumendo, la sintesi multigrammo ottimizzata del frammento C9-C16 8 è stata completata in 10 passaggi con una resa totale del 43% dall'estere di partenza (S)-13.
La conversione del lattone 24 ad aril estere 8 era ora richiesta (Schema 4). Inizialmente, è stata impiegata una sequenza di quattro passaggi, in base a cui la metanolosi del 24 e la protezione come TBS del risultante idrossi estere ha fornito il 26 (84%, 2 passaggi), e la saponificazione e l'esterificazione con 2,6-dimetilfenolo nelle condizioni di Steglich25 ha fornito il frammento chiave 8 (78%, 2 passaggi).
Successivamente, una più corta sequenza di tre passaggi è stata impiegata per ottenere il frammento chiave 8 con una resa totale dell'81%. Questa comportava la diretta apertura del lattone 24 ad idrossi acido intermedio ed esterificazione25 con 2,6-dimetilfenolo a dare l'idrossi estere 27, seguita da protezione come TBS a dare 8. Riassumendo, la sintesi multigrammo ottimizzata del frammento C9-C16 8 è stata completata in 10 passaggi con una resa totale del 43% dall'estere di partenza (S)-13.
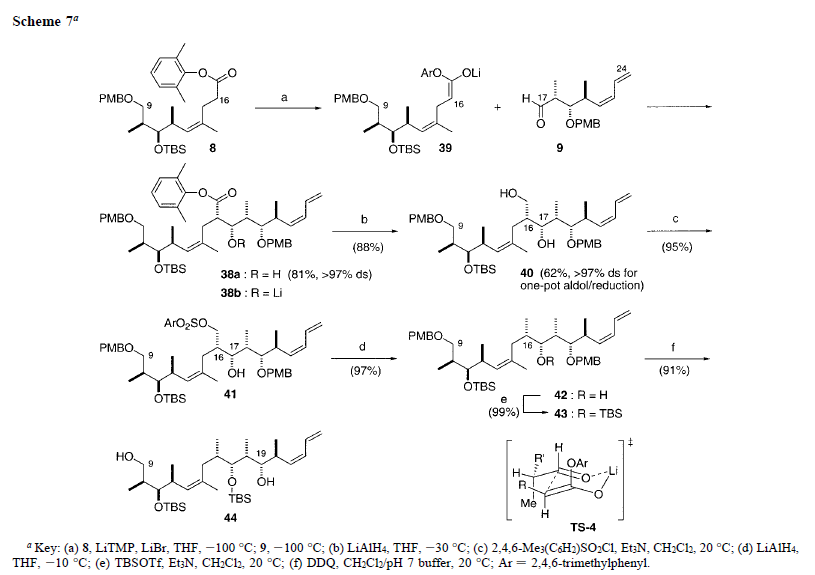
 Sintesi della subunità C17-C24, 9. La sintesi del frammento C17-C24 9 ha richiesto l'unione di due partner di coupling chirali per configurare la stereotriade (Schema 5).
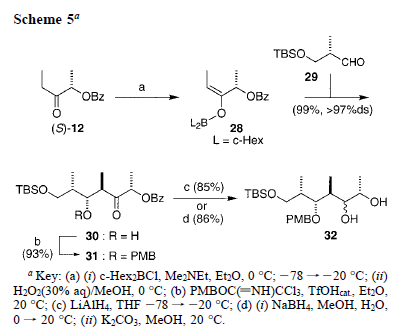
L'etil chetone (S)-12 è stato preparato in tre passaggi dall'etil (S)-lattato, disponibile commercialmente, con una resa del 65%, come precedentemente descritto16a. L'enolizzazione del chetone (S)-12, usando (c-Hex)2BCl/Me2NEt, genera esclusivamente l'enolato (E) di boro 28. L'aggiunta dell'aldeide α-chirale 29 (preparata da (S)-13) fornisce, dopo workup ossidativo, il prodotto aspettato anti-aldolo 30 con eccellente resa e selettività (99%, >97% ds)16,26. Condizioni ottimali richiedono un eccesso di 1.5-volte, fino a 2-volte, di aldeide 29 rispetto all'enolato. Dopo una considerevole sperimentazione, la protezione del gruppo β-idrossi è stata ottenuta usando p-metossibenzil-tricloroacetimidate ad elevata purezza ed acido triflico (0.3 mol %) a dare il chetone 31 con una resa del 93%27. Con il chetone protetto a disposizione, la conversione all'1,2-diolo 32 era ora necessaria.
Questa è stata ottenuta tramite uno dei due metodi: (i) riduzione con
LiAlH4 (85%) o (ii) riduzione del chetone (NaBH4) seguita da idrolisi del benzoato (K2CO3, MeOH) (86%), dove l'ultima procedura fornisce un qualcosa in più per una sintesi multigrammo16.
Sintesi della subunità C17-C24, 9. La sintesi del frammento C17-C24 9 ha richiesto l'unione di due partner di coupling chirali per configurare la stereotriade (Schema 5).
L'etil chetone (S)-12 è stato preparato in tre passaggi dall'etil (S)-lattato, disponibile commercialmente, con una resa del 65%, come precedentemente descritto16a. L'enolizzazione del chetone (S)-12, usando (c-Hex)2BCl/Me2NEt, genera esclusivamente l'enolato (E) di boro 28. L'aggiunta dell'aldeide α-chirale 29 (preparata da (S)-13) fornisce, dopo workup ossidativo, il prodotto aspettato anti-aldolo 30 con eccellente resa e selettività (99%, >97% ds)16,26. Condizioni ottimali richiedono un eccesso di 1.5-volte, fino a 2-volte, di aldeide 29 rispetto all'enolato. Dopo una considerevole sperimentazione, la protezione del gruppo β-idrossi è stata ottenuta usando p-metossibenzil-tricloroacetimidate ad elevata purezza ed acido triflico (0.3 mol %) a dare il chetone 31 con una resa del 93%27. Con il chetone protetto a disposizione, la conversione all'1,2-diolo 32 era ora necessaria.
Questa è stata ottenuta tramite uno dei due metodi: (i) riduzione con
LiAlH4 (85%) o (ii) riduzione del chetone (NaBH4) seguita da idrolisi del benzoato (K2CO3, MeOH) (86%), dove l'ultima procedura fornisce un qualcosa in più per una sintesi multigrammo16.
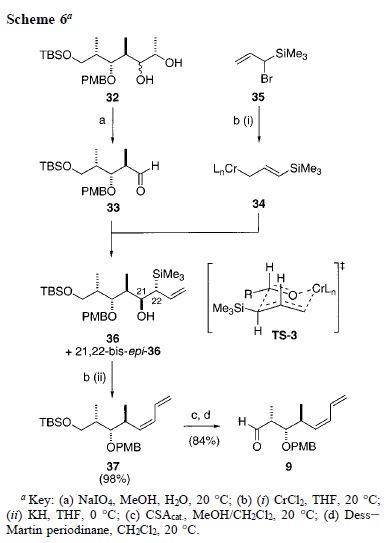
 L'introduzione dell'unità (Z)-dienica terminale C21-C24 della discodermolide è stata ottenuta in modo davvero efficiente seguendo un precedente protocollo sviluppato dagli autori11h. Questo ha richiesto prima, la rottuta ossidativa dell'1,2-diolo 32 con NaIO4 a dare l'aldeide 33 (Schema 6). La reazione di Nozaki-Hiyama tra l'aldeide grezza 33 ed il reagente di allil cromo 34, generato in situ dall'1-bromo-1-trimetilsilil-2-propene 35 e cloruro di cromo(II) in THF28 ha fornito (tramite TS-3) l'anti β-idrossi silano intermedio 36. Questi prodotti grezzi sono stati quindi direttamente sottoposti ad una syn eliminazione tipo Peterson29 con KH in THF, a dare esclusivamente il desiderato diene (Z) 37 con rese eccellenti (98% dal 32). La deprotezione del TBS etere (CSA, MeOH/CH2Cl2) e l'ossidazione col Dess-Martin30 dell'alcole intermedio hanno completato la sintesi dell'aldeide dienica C17-C24 9 (84%, 2 passaggi). Riassumento, la sintesi ottimizzata del frammento chiave 9 dall'etil (S)-lattato è stata portata a termine in 10 passaggi con una resa totale del 42%, su una scala multigrammo.
L'introduzione dell'unità (Z)-dienica terminale C21-C24 della discodermolide è stata ottenuta in modo davvero efficiente seguendo un precedente protocollo sviluppato dagli autori11h. Questo ha richiesto prima, la rottuta ossidativa dell'1,2-diolo 32 con NaIO4 a dare l'aldeide 33 (Schema 6). La reazione di Nozaki-Hiyama tra l'aldeide grezza 33 ed il reagente di allil cromo 34, generato in situ dall'1-bromo-1-trimetilsilil-2-propene 35 e cloruro di cromo(II) in THF28 ha fornito (tramite TS-3) l'anti β-idrossi silano intermedio 36. Questi prodotti grezzi sono stati quindi direttamente sottoposti ad una syn eliminazione tipo Peterson29 con KH in THF, a dare esclusivamente il desiderato diene (Z) 37 con rese eccellenti (98% dal 32). La deprotezione del TBS etere (CSA, MeOH/CH2Cl2) e l'ossidazione col Dess-Martin30 dell'alcole intermedio hanno completato la sintesi dell'aldeide dienica C17-C24 9 (84%, 2 passaggi). Riassumento, la sintesi ottimizzata del frammento chiave 9 dall'etil (S)-lattato è stata portata a termine in 10 passaggi con una resa totale del 42%, su una scala multigrammo.