Martilla
2018-12-09 16:39
Calcolare la solubilità dei tre cromati poco solubili a pH 4.
I cromati sono : CaCro4 , BaCrO4, SrCrO4.
Allego la mia soluzione. Per favore, qualcuno potrebbe controllarlo? Grazie.
CaCrO4(s) 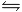 Ca2+ + CrO4(2-)...........Ks CaCrO4 = 7,1·10^-4
SrCrO4(s)
Ca2+ + CrO4(2-)...........Ks CaCrO4 = 7,1·10^-4
SrCrO4(s) 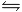 Sr2+ + CrO4(2-)............Ks SrCrO4 = 2,0·10^-5
BaCrO4(s)
Sr2+ + CrO4(2-)............Ks SrCrO4 = 2,0·10^-5
BaCrO4(s) 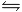 Ba2+ + CrO4(2-)...........Ks BaCrO4 = 1,2·10^-10
CrO4(2-) + H+
Ba2+ + CrO4(2-)...........Ks BaCrO4 = 1,2·10^-10
CrO4(2-) + H+ 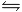 HCrO4(-)
HCrO4(-) + H+
HCrO4(-)
HCrO4(-) + H+ 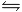 H2CrO4
Comincio dal calcio.
Mi calcolo il kps in ambiente acido,
Kps (acido) = kps/ kw x ka1 => (7.1x10^-4)/ (10^14) x (0,18) => 3,94x10^11
S = [H+] x radice(kps acido) => 62,80 M
Per lo Sr ho eseguito lo stesso procedimento e la solubilità è pari a 10,54 M
Mentre per il Ba, s= 0,026 M
Teoricamente dovrebbe andare bene, visto che la solubilità dovrebbe decrescere in questo ordine considerati i kps però non so se ho impostato bene l’esercizio.
H2CrO4
Comincio dal calcio.
Mi calcolo il kps in ambiente acido,
Kps (acido) = kps/ kw x ka1 => (7.1x10^-4)/ (10^14) x (0,18) => 3,94x10^11
S = [H+] x radice(kps acido) => 62,80 M
Per lo Sr ho eseguito lo stesso procedimento e la solubilità è pari a 10,54 M
Mentre per il Ba, s= 0,026 M
Teoricamente dovrebbe andare bene, visto che la solubilità dovrebbe decrescere in questo ordine considerati i kps però non so se ho impostato bene l’esercizio.

