Magno
2019-01-21 10:30
Ciao a tutti,
1) devo calcolare il pH di una soluzione di HF 0.4M,
2) successivamente calcolare la variazione di pH aggiungendo 1g di NaF a 25mL, non considerando la variazione di volume.
non avendo dati sulla Ka e pH iniziali li ho ricavati delle tabelle:
Ka = 7,2 * 10ˉ⁴
pH = - log (√7,2 * 10ˉ⁴ * 0,4M) = 1,77
all'eq dopo l'aggiunta:
HF 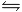 H⁺ + F⁻
H⁺ + F⁻
0.4M x 0.952 mol/L (1g / 42g/mol) / 0.025L = 0.952mol/L
da cui 7,2 * 10ˉ⁴ = [H⁺] * 0.952/0.4 =>
[H⁺]= 0.00072 * 0.4/0.952 = 0.0003 mol/L
pH = - log 0.0003 = 3.52
∆pH = 3.52 - 1.77 = 1.75
Ci sono degli errori?