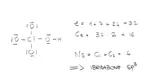marco_1004
2017-07-17 06:43
Mi servirebbe una mano nel determinare alcune formule di struttura. Per farlo utilizzo il metodo VSEPR, seguendo questi passaggi:
1. Calcolare il numero totale di elettroni e
2. Calcolare il numero di coppie elettroniche ce = e : 2
3. Assegnare le coppie di legame cl (pari al numero di atomi legati all’atomo centrale)
4. Completare l’ottetto degli atomi legati a quello centrale
5. Assegnare le restanti coppie elettroniche cs (Ione pairs) all’atomo centrale
6. Calcolare Il numero sterico NS = cl + cs
Ad esempio HClO4
abbiamo in totale 32 elettroni, ovvero 16 coppie.
Tuttavia da quanto ho capito una volta fatti i passaggi sopra elencati determino si la struttura molecolare e l'ibridazione dell'atomo centrale, se dovessi però calcolare l'ibridazione degli altri atomi dovrei fare un passaggio in più andando a calcolare la carica formale giusto??
La motivazione di questo passaggio in più necessario è che ai fini dell'ibridazione della struttura a noi interessano le coppie solitare (ione pairs) e i legami 𝜎 dell'atomo centrale, infatti eventuali legami 𝜋 con gli atomi legati a quello centrale non vanno a modificare nè l'ibridazione nè la struttura molecolare.
Tuttavia essi modificano l'ibridazione degli atomi "periferici", infatti nel nostro caso se uno degli ossigeni forma con il cloro un doppio legame, esso avrà due ione pairs e un legame 𝜎 mentre invece nel caso in cui formasse un legame semplice avrebbe 3 ione pairs e un legame 𝜎, quindi si avrebbero rispettivamente ibridazione sp2 e sp3.
in questo caso ho:
Cl: 7 - 0 - 4 = +3
O: 6 - 6 - 1 = - 1
OH : 6 - 4 - 2 = 0
A questo punto quindi si ha la seguente situazione:
quindi per neutralizzare la carica positiva sul cloro gli ossigeni formano dei doppi legami. La struttura molecolare resta la stessa infatti il Cloro formerà comunque 4 legami 𝜎 , tuttavia è cambiata l'ibridazione degli ossigeni periferici.... corretto?