Paola17
2019-02-14 11:41
Ciao  ho cercato di svolgere il seguente problema, ma con scarsi risultati. Ho bisogno di una mano per risolverlo. Vi allego il problema e ciò che sono riuscita a fare(pochissimo)
ho cercato di svolgere il seguente problema, ma con scarsi risultati. Ho bisogno di una mano per risolverlo. Vi allego il problema e ciò che sono riuscita a fare(pochissimo)
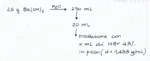
Calcolare il volume di una soluzione di acido bromidrico al 48% (d=1,488 g/cm3) necessario a titolare 20cm3 di una soluzione di idrossido di bario ottenuta sciogliendo 2,6g del sale in 250cm3 di acqua.
2HBr + Ba(OH)2 —> BaBr2 + 2H2O
Moli Ba(OH)2= 2,6g/171,34= 0,015moli
Rapporto di 1:2 con 2HBr che sarà 0,03 moli
Grazie