quimico
2011-11-11 09:42
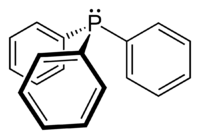
La trifenilfosfina (Ph3P) è un reagente molto versatile ampiamente usato dai chimici organici. Ph3P esiste a temperatura ambiente sotto forma di cristalli stabili all'aria, incolori. Si scioglie in solventi organici non polari come il benzene e dietiletere. Ph3P subisce lenta ossidazione da parte dell'aria a dare il trifenilfosfinossido, Ph3P=O. Questa impurità può essere rimossa tramite ricristallizzazione della Ph3P o da etanolo caldo o isopropanolo caldo1.
Negli anni recenti Ph3P ha ricevuto un'attenzione crescente quale reagente versatile e blando in molte occasioni per diverse trasformazioni organiche in condizioni neutre2.
Le proprietà che suggeriscono il suo uso sono la sua nucleofilicità ed il suo carattere riducente3. La nucleofilicità della Ph3P è indicata dalla sua reattività nei confronti di alcheni elettrofili come gli accettori di Michael4 e gli alogenuri alchilici5.
La Ph3P lega bene la maggior parte dei metalli di transizione, specialmente quei metalli della middle e late transition dei gruppi 7–106.
 A Zhou et al. riportarono l'isomerizzazione di alchinil chetoni catalizzata da Ph3P in acqua in assenza di solvente organico, la quale fornì un metodo pratico per la sintesi degli utili composti polienil carbonilici. Sono stati ottenuti (E,E)-diene chetoni con buone rese quando la reazione veniva condotta a riflusso in mezzi acquosi7.
A Zhou et al. riportarono l'isomerizzazione di alchinil chetoni catalizzata da Ph3P in acqua in assenza di solvente organico, la quale fornì un metodo pratico per la sintesi degli utili composti polienil carbonilici. Sono stati ottenuti (E,E)-diene chetoni con buone rese quando la reazione veniva condotta a riflusso in mezzi acquosi7.
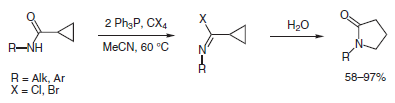
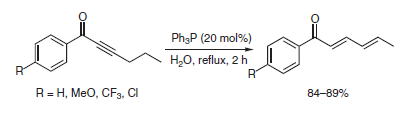 B Yang e Shi ebbero successo nell'attivazione di ciclopropil ammidi (ciclopropani monoattivati) attraverso i corrispondenti imidoil alogenuri preparati in situ in presenza di 2 equiv di Ph3P e di 1 equiv di CX4, portando a prodotti di espansione di anello (pirrolidin-2-oni N-sostituiti) con buone rese8.
B Yang e Shi ebbero successo nell'attivazione di ciclopropil ammidi (ciclopropani monoattivati) attraverso i corrispondenti imidoil alogenuri preparati in situ in presenza di 2 equiv di Ph3P e di 1 equiv di CX4, portando a prodotti di espansione di anello (pirrolidin-2-oni N-sostituiti) con buone rese8.
 C La reazione di diversi alcoli con 2.5 equiv di Ph3P e con una quantità equimolare di N-fluorodibenzenesulfonimmide ha portato alle corrispondenti dibenzenesulfonimmidi. La reazione porta a rese elevate nel caso in cui i substrati sono alcoli primari9.
C La reazione di diversi alcoli con 2.5 equiv di Ph3P e con una quantità equimolare di N-fluorodibenzenesulfonimmide ha portato alle corrispondenti dibenzenesulfonimmidi. La reazione porta a rese elevate nel caso in cui i substrati sono alcoli primari9.
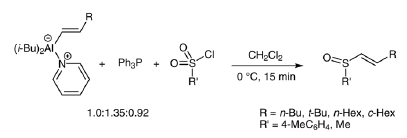
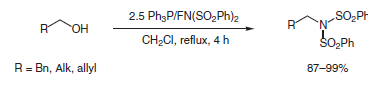 D La reazione tra complessi alano-piridina, Ph3P, e solfonil cloruri fornisce gli aril 1-alchenil solfossidi con rese da buone ad eccellenti (70–94%) in brevi tempi di reazione usando condizioni blande. Il rapporto ottimale tra i reagenti (alano-piridina/Ph3P/solfonil cloruro = 1.00:1.35:0.92) è stato ottenuto eseguendo un analisi chemiometrica3.
D La reazione tra complessi alano-piridina, Ph3P, e solfonil cloruri fornisce gli aril 1-alchenil solfossidi con rese da buone ad eccellenti (70–94%) in brevi tempi di reazione usando condizioni blande. Il rapporto ottimale tra i reagenti (alano-piridina/Ph3P/solfonil cloruro = 1.00:1.35:0.92) è stato ottenuto eseguendo un analisi chemiometrica3.
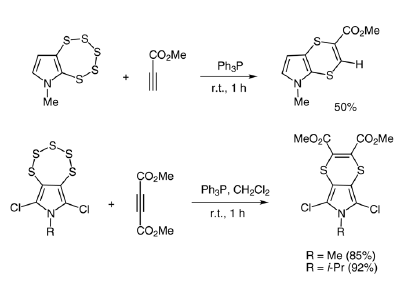
 E Le 1,2,3,4,5-pentatiepine fuse con sistemi aromatici ed eterocicliche reagiscono con trifenilfosfina ed alchini che portano gruppi elettron-attrattori a dare le corrispondenti 1,4-ditiine con ottime rese. Alchini non simmetrici addizionano regioselettivamente a dare prodotti in accordo con la distribuzione elettronica in un intermedio di reazione proposto10.
E Le 1,2,3,4,5-pentatiepine fuse con sistemi aromatici ed eterocicliche reagiscono con trifenilfosfina ed alchini che portano gruppi elettron-attrattori a dare le corrispondenti 1,4-ditiine con ottime rese. Alchini non simmetrici addizionano regioselettivamente a dare prodotti in accordo con la distribuzione elettronica in un intermedio di reazione proposto10.
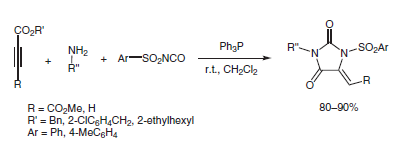
 F Alizadeh e Sheikhi mostrarono un'efficace via di sintesi per i derivati dell'idantoina funzionalizzati, che coinvolgeva la reazione di un derivato dell'urea risultante dall'addizione di un'amina primaria con un arilsulfonil isocianato, ed un alchil propiolato o un dialchil acetilenedicarbossilato in presenza di trifenilfosfina. L'intermedio reattivo 1:1 ottenuto dall'addizione della trifenilfosfina all'alchil propiolato o al dialchil acetilenedicarbossilato è stato intrappolato da NH-acidi quali il derivato dell'urea per produrre i derivati funzionalizzati dell'idantoina11.
F Alizadeh e Sheikhi mostrarono un'efficace via di sintesi per i derivati dell'idantoina funzionalizzati, che coinvolgeva la reazione di un derivato dell'urea risultante dall'addizione di un'amina primaria con un arilsulfonil isocianato, ed un alchil propiolato o un dialchil acetilenedicarbossilato in presenza di trifenilfosfina. L'intermedio reattivo 1:1 ottenuto dall'addizione della trifenilfosfina all'alchil propiolato o al dialchil acetilenedicarbossilato è stato intrappolato da NH-acidi quali il derivato dell'urea per produrre i derivati funzionalizzati dell'idantoina11.
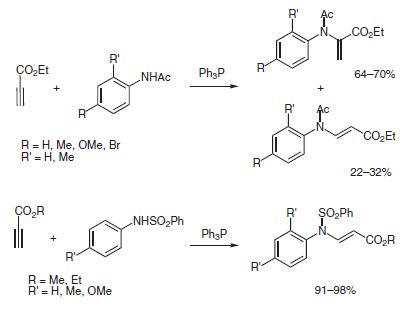
 G L'addizione di acetanilidi ad etil propiolato procede in condizioni neutre in presenza di trifenilfosfina a dare i corrispondenti alchil acrilati β-sostituiti assieme a quantità variabili dell'isomero β-sostituito con geometria E. L'addizione di arilsulfonilanilidi ad alchil propiolati in condizioni simili, ha prodotto solo gli alchil (E)-3-arilsulfonilanilino-2-propenoati8.
G L'addizione di acetanilidi ad etil propiolato procede in condizioni neutre in presenza di trifenilfosfina a dare i corrispondenti alchil acrilati β-sostituiti assieme a quantità variabili dell'isomero β-sostituito con geometria E. L'addizione di arilsulfonilanilidi ad alchil propiolati in condizioni simili, ha prodotto solo gli alchil (E)-3-arilsulfonilanilino-2-propenoati8.
 Riferimenti:
(1) Corbridge, D. E. C. Phosphorus: An Outline of its Chemistry, Biochemistry, and Technology, 5th ed.; Elsevier: Amsterdam, 1995, 68.
(2) Yadav, J. S.; Reddy, B. V. S.; Krishna, A. D.; Reddy, Ch. S.; Narsaiah, A. V. J. Mol. Catal. A: Chem. 2007, 261, 93.
(3) Signore, G.; Calderisi, M.; Malanga, C.; Menicagli, R. Tetrahedron 2007, 63, 177.
(4) a) Bhuniya, D.; Mohan, S.; Narayanan, S. Synthesis 2003, 1018. b) Luis, A. L.; Krische, M. J. Synthesis 2004, 2579. c) Bensa, D.; Rodriguez, J. Synth. Commun. 2004, 34, 1515.
(5) Sato, A.; Yorimitsu, H.; Oshima, K. J. Am. Chem. Soc. 2006, 128, 4240.
(6) Yavari, I.; Hazeri, N.; Maghsoodlou, M. T.; Souri, S. J. Mol. Catal. A: Chem. 2007, 264, 313.
(7) Zhou, Q. F.; Yang, F.; Guo, Q. X.; Xue, S. Chin. Chem. Lett. 2007, 18, 1029.
(8) Yang, Y.; Shi, M. J. Org. Chem. 2005, 70, 8645.
(9) Giovanelli, E.; Doris, E.; Rousseau, B. Tetrahedron Lett. 2006, 47, 8457.
(10) Amelichev, S. A.; Konstantinova, L. S.; Obruchnikova, N. V.; Rakitin, O. A.; Rees, C. W. Org. Lett. 2006, 8, 4529.
(11) Alizadeh, A.; Sheikhi, E. Tetrahedron Lett. 2007, 48, 4887.
Riferimenti:
(1) Corbridge, D. E. C. Phosphorus: An Outline of its Chemistry, Biochemistry, and Technology, 5th ed.; Elsevier: Amsterdam, 1995, 68.
(2) Yadav, J. S.; Reddy, B. V. S.; Krishna, A. D.; Reddy, Ch. S.; Narsaiah, A. V. J. Mol. Catal. A: Chem. 2007, 261, 93.
(3) Signore, G.; Calderisi, M.; Malanga, C.; Menicagli, R. Tetrahedron 2007, 63, 177.
(4) a) Bhuniya, D.; Mohan, S.; Narayanan, S. Synthesis 2003, 1018. b) Luis, A. L.; Krische, M. J. Synthesis 2004, 2579. c) Bensa, D.; Rodriguez, J. Synth. Commun. 2004, 34, 1515.
(5) Sato, A.; Yorimitsu, H.; Oshima, K. J. Am. Chem. Soc. 2006, 128, 4240.
(6) Yavari, I.; Hazeri, N.; Maghsoodlou, M. T.; Souri, S. J. Mol. Catal. A: Chem. 2007, 264, 313.
(7) Zhou, Q. F.; Yang, F.; Guo, Q. X.; Xue, S. Chin. Chem. Lett. 2007, 18, 1029.
(8) Yang, Y.; Shi, M. J. Org. Chem. 2005, 70, 8645.
(9) Giovanelli, E.; Doris, E.; Rousseau, B. Tetrahedron Lett. 2006, 47, 8457.
(10) Amelichev, S. A.; Konstantinova, L. S.; Obruchnikova, N. V.; Rakitin, O. A.; Rees, C. W. Org. Lett. 2006, 8, 4529.
(11) Alizadeh, A.; Sheikhi, E. Tetrahedron Lett. 2007, 48, 4887.
I seguenti utenti ringraziano quimico per questo messaggio: AgNO3, Wavvorov