valeg96
2017-12-03 09:54
In questo thread vedremo rapidamente cos'è una zeolite, che caratteristiche possiede, come è possibile produrne qualche grammo in due modi e come è possibile quantificarne alcune proprietà.
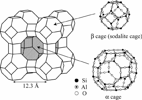
Una zeolite è fondamentalmente un alluminosilicato dotato di una struttura tridimensionale estremamente regolare e ripetitiva, dotata di canali e varie strutture geometriche capaci di inglobare e intrappolare acqua, ioni e piccole molecole (i setacci molecolari per rimuovere tracce d'acqua dai solventi organici non sono altro che zeoliti pressate a forma di sfera e disidratate che inglobano l'acqua presente nel solvente).
La formula generale di una zeolite è parecchio confusa e variegata:
Mn+ x/n[(SiO2)y(AlO2)x]·mH2O
M = catione con carica n+ (H+, Li+, Na+, K+, Ca2+, Mg2+, Ba2+, Sr2+) che neutralizza le cariche negative sul reticolo.
x + y = numero di tetraedri per unità di cella cristallografica.
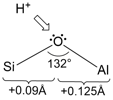
Tra le parentesi quadre si mette in evidenza il contenuto dell’impalcatura tetraedrica (parte rigida) e il rimanente è il contenuto delle cavità, ovvero la parte mobile. In sostanza, la loro unità base è una lunga serie di tetraedri Si e Al legati assieme da ponti ossigeno non lineari e disposti in una struttura tridimensionale strettamente legata al rapporto Si/Al della zeolite.
Le zeoliti possono subire sostituzioni al reticolo di altri atomi, ad esempio:
• Al3+ può essere sotituito da B3+, Ga3+, Fe3+, Cr3+;
• Si4+ può essere sotituito da Ge4+, Ti4+;
• Al3+ e Si4+ possono essere sotituiti da P3+ a formare SAPO, zeoliti silicoalluminofosfate.
Le zeoliti hanno proprietà notevolmente interessanti per la ricerca e l’industria, e in particolare:
• Subiscono disidratazione reversibile;
• Sono molto selettive verso ioni o molecole specifiche: offrono un eccellente adsorbimento di acqua o piccole molecole organiche e un buon scambio cationico;
• Possono essere impiegate a fini catalitici;
• Hanno bassa densità, buona resistenza meccanica e alta permeabilità;
• Hanno solitamente costi di produzione contenuti rispetto alle resine sintetiche.
Zeoliti equimolari in Si e Al, come la zeolite A (con rapporto Si/Al = 1) sono abbastanza delicate verso le temperature superiori ai 150°C e sono ricche di siti acidi, caricati negativamente (grazie alla presenza di Al) e disposti a inglobare efficacemente cationi e piccole molecole polari. Zeoliti con un rapporto Si/Al fino a 5, ovvero con fino a 5 volte più Si di Al sono più resistenti alle temperature e possiedono discrete caratteristiche catalitiche. Zeoliti ad alto tenore di silice, con Si/Al fino a 100 sono pressoché costituite da silicio puro, non hanno alcuna tendenza ad adsorbire cationi e molecole polari, sono resistenti fino anche a 1000°C e presentano enorme affinità per gli idrocarburi.
Le zeoliti acide (delle quali parleremo in questa sede) hanno l'interessante caratteristica di poter catturare alcuni ioni a discapito di altri adsorbendoli all'interno dei canali o delle strutture tridimensionali, modificando leggermente la loro matrice. Questa caratteristica le rende componenti essenziali di ogni detersivo al fine di sequestrare ioni Ca2+ e Mg2+ per ridurre la durezza dell'acqua e migliorare le prestazioni del prodotto. E' possibile estrarre le zeoliti da un detersivo in polvere da bucato, ma si tratta di una procedura dispendiosa e lunga, che consuma notevoli quantità di acetone e acqua distillata (brevemente, si acidifica il detersivo sciolto in acqua per precipitare la zeolite, si decanta e si lava accuratamente con acetone per rimuovere tensioattivi e quant'altro).
Le zeoliti sono un commodity chemical, ovvero un reagente chimico prodotto in massive quantità da impianti dedicati, e trovano applicazioni in svariati campi, dalla decalcificazione all'anidrificazione fino alla catalisi chimica. La loro grande economicità (tranne che nel caso delle zeoliti per catalisi) deriva dal fatto che è possibile produrre zeolite abbastanza rapidamente da materie prime di scarso valore senza incappare in reflui tossici e reagenti pericolosi, producendo un prodotto dai molteplici usi e assolutamente ecocompatibile (esistono circa 40 zeoliti naturali da collezione e qualche centinaio di zeoliti sintetiche).
1. ZEOLITE A da idrogel
La sintesi da idrogel opera unendo due o più soluzioni contenenti le specie fondamentali alla zeolite. Le specie sono quindi solubili e andranno a formare un idrogel dopo essere unite ed agitate, che avrà tempo di cristallizzare in una stufa a non più di 100°C per almeno 2-4h. Le due soluzioni utilizzate hanno rapporto Si/Al 1:1 (circa 0.06mol), che corrisponde ad una zeolite A. La prima soluzione è composta da gel di silice in polvere solubilizzato da NaOH a formare metasilicato di sodio, la seconda contiene alluminio(III) isopropossido, un sale solubile di alluminio relativamente facile da produrre (vedere NileRed)
Soluzione 1 mNaOH = 2.3126g mSiO2 = 4.0759g
Soluzione 2 mNaOH = 2.3290g mAl(iP)3 = 10.2312g
Le due soluzioni sono unite e agitate per 10min a temperatura ambiente (RT), al fine di favorire la formazione di idrogel (si osservano due fasi distinte). L'idrogel è trasferito in un contenitore di HDPE (quelli classici quadrati o rotondi della Kartell) con l'aiuto di qualche aliquota di acqua deionizzata (DI) (circa 20-30mL, non di più) e lasciato in stufa a 105°C con tappo socchiuso per 24h. Si filtra, lava su buchner con molta (almeno 100-500mL) acqua DI e si procede alle caratterizzazioni. La resa è pressoché quantitativa.
2. ZEOLITE A da metacaolino
Questa sintesi è industrialmente molto più economica della prima, in quanto costa meno calcinare un minerale economico (caolino) che acquistare tonnellate di alluminio isopropossido e gel di silice puri. La sintesi si basa sull'assunto che se la zeolite è un alluminosilicato artificiale ben disposto tridimensionalmente nulla ci vieta di prendere un alluminosilicato naturale, economico e a composizione definita, rompere o indebolire in qualche modo il suo reticolo e costringerlo a riarrangiarsi in forma zeolitica.
A questo proposito si impiega il caolino, un alluminosilicato economico e dai molteplici usi in farmacia, porcellane, intonaci e quant'altro sotto il nome di argilla bianca. Vi è un inconveniente: il caolino è un minerale estremamente stabile e resistente all'attacco chimico, e per renderlo reattivo bisogna calcinarlo a 600-800°C per trasformarlo a metacaolino. Il metacaolino contiene a questo punto tutti gli elementi necessari alla produzione di zeolite A, e Si/Al = 1.
Al2Si2O5(OH)4 → Al2Si2O7
Si calcina una decina di grammi di caolino di grado farmaceutico (con tracce di CaO <0.5%) a 610°C per circa 24h.
Secondo Ayele, Pérez-Pariente et al., ed altre fonti, la zeolite A migliore si ottiene con un rapporto metacaolino/NaOH(aq) di 5g/100mL e il grado di cristallinità aumenta con la concentrazione di NaOH, impiegata in un range tra 1M e 3M.
Seguendo la letteratura, 2.50g di metacaolino e 50mL di NaOH 3M sono uniti ed agitati per 10min RT. Segue poi un risposo a RT per 3gg e un periodo di maturazione in stufa a 105°C per 24h. La zeolite è filtrata su buchner, lavata con circa 200mL di acqua DI e seccata in stufa a 105°C. Si procede alle caratterizzazioni. La resa è pressoché quantitativa.

L'impiego principale della zeolite è come sequestrante di ioni e piccole molecole, e perciò trova impiego sotto forma di setacci molecolari o polveri decalcificanti nei detersivi in polvere. L'efficienza di una zeolite (o di una sostanza più generica, come una resina a scambio ionico, un'argilla o un polimero) nello scambiare ioni è definita CSC, CSI o CS, capacità di scambio cationico, ionico o generico, misurata in meq/g o meq/ml a seconda dei casi. La metodica è semplice: si pesa una quantità di zeolite, la si lascia in agitazione in una soluzione a titolo noto del nostro analita, in questo caso Ca2+ per un intervallo di tempo definito, in questo caso 10 minuti circa.
3. CAPACITA’ DI SCAMBIO DELLE ZEOLITI
La capacità di scambio della zeolite A da idrogel è stata misurata su 0.2021g di zeolite ben secca lasciati in agitazione a RT in 75mL CaCl2 0.00936M. La sospensione viene filtrata su gooch dopo 10min e portata a 100mL in un matraccio classe A. Si titolano 25mL con EDTA 0.01M ed EBT 10% in NaCl.
V CaCl2 = 75mL
C EDTA = 0.01M
V prelevato = 25mL
V X = 9.8mL
eq CaCl2 Iniziali = 75mL·0.00936M·2eq/mol = 1.40meq
eq CaCl2 Finali = 9.8mL·0.01M·4·2eq/mol = 0.784meq
CSZA Idrogel = (1.40-0.78)meq/0.2021g = 3.07meq/g
La capacità di scambio della zeolite da metacaolino è stata misurata addolcendo 75mL di un campione di acqua dura a 34.81°f con 0.21g di zeolite A sotto agitazione a RT per 15min. Si titolano 20mL della soluzione filtrata su cotone con EDTA 0.01M ed EBT 10% in NaCl.
°f = V EDTA·C EDTA·100.086·(75/20)·(100/75) = V EDTA·C EDTA·100.085·5
°f dura = 34.81°f
°f addolcita = 11.01°f
CSZA Metacaolino = 2eq/mol·(34.81-11.01)/(100.086g/mol·0.21g) = 2.26meq/g
La capacità di scambio di una zeolite A pura si aggira sui 5.48meq/g e diminuisce al diminuire della cristallinità. Essendo la zeolite molto sensibile alle vibrazioni durante la fase di cristallizzazione, questa diminuizione di CS è imputabile alla posizione della stufa, soggetta a vibrazioni, aperture e viavai di persone.
E' lecito domandarsi: se il detersivo in polvere da lavatrice contiene zeoliti, è possibile calcolare la CS del detersivo?
4. CAPACITA’ DI SCAMBIO DEL DETERSIVO
La capacità di scambio di un detersivo in polvere è misurata addolcendo una soluzione di 75mL di CaCl2 0.00933M con 1.0079g di detersivo per 10min. La soluzione è filtrata su buchner, portata a 100mL in un matraccio classe A e titolata ad aliquote.
V CaCl2 = 75mL
C EDTA = 0.00933M
V prelevato = 25mL
V X = 4.7mL
n CaCl2 Iniziali = 0.1L·0.00933M = 0.93mmol
n CaCl2 Finali = n EDTA 0.01M = 4.7mL·0.01M·8 = 0.376mmol
CSDetersivo = 2eq/mol·(0.93-0.38)mmol/1.0079g = 1.09meq/g
I seguenti utenti ringraziano valeg96 per questo messaggio: ClaudioG., ohilà, TrevizeGolanCz, Copper-65, NaClO, luigi_67, AndreaChem, EdoB