LucaZombini
2020-09-09 15:24
25,62 g di N2O4 sono posti in un sistema isolato V = 37,3 dm3 mantenuto alla temperatura di 298 K. Calcolare il grado di dissociazione di N2O4
Calcolare inoltre il volume a cui si deve portare il sistema affinchè il grado di dissociazione si dimezzi.
Le soluzioni sono queste
a = 0.3601
V = 7,27 dm3
ho fatto così:
nN2O4 = 25,62/92 = 0,278
PV = nRT -> P = nRT/V
P = 0,0278*0,0821*298/37,3 = 0,18
N2O4 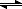 2NO2
2NO2
Kp = p2NO2/pN2O4
0,148 = (2*0,18*α)^2 /0,18(1-α)
α = 0,3621
onestamente, non so come svolgere la seconda parte del problema. Inoltre ho dei dubbi su come abbia calcolato il grado dato che la terza cifra decimale dovrebbe essere 0.
