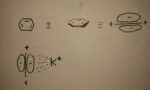zodd01
2017-05-13 16:29
Buonasera,
come ha già spiegato bene quimico, la chimica supramolecolare è la chimica delle interazioni deboli. Le supramolecole infatti si formano e sono tenute insieme da legami non covalenti intermolecolari. In questo post andremo a vedere più da vicino quali sono le interazioni deboli coinvolte, come agiscono, le loro caratteristiche, la loro forza. Gran parte le si conoscono già in chimica generale, altre no, tuttavia qui le vedremo in maggiore dettaglio.
Abbiamo:
1. Interazioni elettrostatiche
1.1. ione – ione
1.2. ione – dipolo
1.3. dipolo – dipolo
2. Legame a idrogeno
3. Forze di dispersione e induzione ( van der Waals )
4. Catione – π
5. CH – π
6. π – π
7. Effetto idrofobico
Iniziamo dalle elettrostatiche che si suddividono a loro volta in 3 tipi. Dipendono dalla permettività del mezzo in cui si trovano, molto forti in fase gassosa meno nei solventi.
IONE – IONE
Sono interazioni regolate dalla legge di Coulomb che ricordiamo essere:
F = 1\e * q1*q2\ d^2
le interazioni ione – ione non sono direzionali, nel senso che in qualunque maniera si dispongano fra loro gli ioni interagenti la forza del legame è sempre uguale. Possono essere attrattive e repulsive. Agiscono relativamente a lunga distanza, diminuendo con essa come 1\r e dipendono dalla permettività del mezzo in cui si trovano, molto forti in fase gassosa mediate invece nei solventi. Un esempio di tale legame è il reticolo del cloruro di sodio.
IONE – DIPOLO
Sono le interazioni che si instaurano fra una molecola polare e uno ione. A differenza delle ione – ione questo tipo di legame è direzionale. Dipendono dall'angolo fra ione e dipolo, dal momento di questo e dalla carica dello ione. Diminuiscono col quadrato della distanza come 1\ r^2. E' importante pure il rapporto carica \ superficie infatti l'entalpia di idratazione degli ioni alcalini diminuisce scendendo lungo il gruppo:
IONE | ENTALPIA IDRATAZIONE ( kcal\mol )
Li+ - 122
Na+ - 98
K+ - 81
Rb+ - 76
Cs+ - 71
________________________________
Un esempio sono gli eteri corona che coordinano cationi alcalini.
DIPOLO – DIPOLO
Le dipolo-dipolo sono fortemente direzionali, a corto raggio, dipendono dal seno e dal coseno dell'angolo formato dai due dipoli. Può formarsi in 2 modi. Prendiamo come esempio 2 molecole di acetone e vediamo che la 1 è presente sia allo stato solido che liquido mentre la 2 solo allo stato solido. La 2 è la più forte e può arrivare a 5 kcal \ mol.
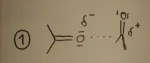
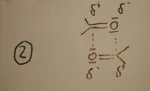
LEGAME A IDROGENO
E’ l’interazione più importante della chimica supramolecolare. Può arrivare oltre 10 kcal\ mol. La possiamo vedere come un caso speciale di interazione dipolo – dipolo. Avviene quando un H è legato a un atomo elettronegativo in grado di polarizzare il legame X – H. E’ direzionale, diminuisce con la distanza come 1\r^3 e in particolare più donatore e accettore stanno sullo stesso asse più è forte il legame. Dagli esempi vediamo che spostandoci dalla linearità del legame le cariche parziali negative iniziano a respingersi indebolendo il legame.
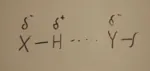
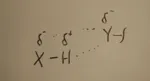
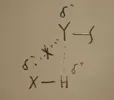
La caratteristica dell'assialità viene dal fatto che il legame a idrogeno è un legame parzialmente covalente. Da calcoli quantomeccanici sull'interazione fra due molecole di acqua si vede che la distanza fra H e O è inferiore alla somma dei raggi di van der Waals ( 1,76 A contro 2,8 A della somma dei raggi ), indice di carattere parzialmente covalente del legame. Discostandosi dalla assialità, ovviamente il legame si indebolisce. E' parzialmente covalente ma il rimanente è elettrostatico, dipolo - dipolo, come detto sopra, ed in quanto tale dipende dall'ambiente in cui si trova, dal solvente, e se questo può fare legami a idrogeno a sua volta, si instaura un equilibrio che indebolisce il legame a idrogeno fra le molecole considerate. Al contrario, in solventi apolari il legame a idrogeno fra 2 molecole è più forte.
Se due molecole hanno più atomi donatori - accettori di H allora possono verificarsi effetti secondari di attrazione repulsione.
In questo caso legami incrociati sono meno forti di legami accoppiati per via delle interazioni diagonali:
D....A D....A
A....D D....A
D....A D....A
Meno forti Più forti
CATIONE – π
E’ l’interazione che si instaura fra un catione e un sistema π che può essere quello di un sistema aromatico, dei doppi legami coniugati o un semplice doppio legame. Prendendo come esempio il benzene, visto di lato, vediamo che la nuvola elettronica rappresenta un δ- mentre sugli idrogeni vi è un δ+, a motivo della maggiore elettronegatività dei carboni sp2 rispetto a quelli degli sp3.
La nuvola elettronica può così coordinare cationi ed è stata misurata l’interazione del benzene con diversi cationi metallici in fase gas.
IONE | E binding ( kcal \ mol )
Li+ 38
Na+ 27
K+ 19
Rb+ 16
_____________________
I sostituenti sull'anello benzenico possono perturbare il sistema aromatico variandone la capacità di interazione. Sotto un esempio con l'interazione tra benzeni e ione sodio in fase gassosa. Si vede che sostituenti elettron attrattori diminuiscono l'energia di interazione mentre i donatori la aumentano.
COMPOSTO | E binding ( kcal \ mole )
benzene 27,1
fluorobenzene 22,0
cianobenzene 15,7
anilina 31,8
fenolo 26,9
___________________________________
DIPOLO \ CH – π
Si instaura fra un sistema π e un dipolo che può essere quello di una molecola polare o un C-H polarizzato per effetto induttivo da un gruppo elettronattrattore legato al carbonio come può essere nel nitrometano. L'energia di binding fra il benzene e alcune molecole polari è mostrata sotto:
COMPOSTO | E binding ( kcal\mol )
Acqua 1,9
Ammoniaca 1,4
Anilina 1,6
STACKING π-π
A sua volta anche 2 sistemi π fra loro possono instaurare una interazione che fra le π è addirittura la più forte arrivando a 1,5 kcal \ mol. Essi possono interagire in 2 modi: face to face ed edge to face, quest’ultima adottata dal benzene solido. Nella face to face i due sistemi sono impilati fra loro ma sfalsati di modo che il δ+ sull’idrogeno vada a centrare la nuvola del sistema adiacente. E’ la struttura adottata dalla grafite. Nella edge to face si ha invece che l’idrogeno del bordo punti al centro della nuvola del secondo sistema formando una T.

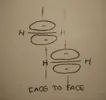

Una disposizione impilata eclissata si ottiene fra esafluorobenzene e benzene. Nell'esafluorobenzene si ha una vera e propria inversione di polarità, con un bordo ricco di elettroni e l'anello carente. L'interazione supramolecolare col benzene è molto forte, il complesso solido formato è detto a trasferimento di carica, ha un punto di fusione di 24°C contro i 5,5°C del benzene e i 4°C dell'esafluoro come se fosse un composto completamente differente. Composti del genere si formano quando un donatore e un accettore hanno HOMO e LUMO molto vicini energeticamente. E' una vera e propria donazione di densità elettronica dal donatore all'accettore. Negli spettri UV-VIs di tali composti appare una banda molto larga e intensa detta a trasferimento di carica. Un altro esempio è il solido porpora formato da esametilbenzene e tetracianoetilene.
FORZE DI VAN DER WAALS INDUZIONE \ DISPERSIONE
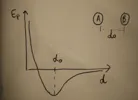
Si realizzano fra molecole poco polari o apolari. Sono dovute ad attrazioni per dipolo istantaneo – dipolo indotto o dipolo - dipolo indotto. Sono molto deboli, inferiori a 0,4 kcal \ mol. Azoto o ossigeno liquido sono tenuti insieme da interazioni del genere. Aumentano con la polarizzabilità, la dimensione e la superficie esposta ( forma ). Dipendono pure dalla distanza dove sono attrattive fino a un minimo per poi diventare repulsive al di sotto di quel minimo.
EFFETTO IDROFOBICO
Sono molto importanti in chimica supramolecolare, alla base di questo tipo di interazioni ci stanno le forze di van der Waals. Esistono due tipi di effetto idrofobico detti classico e non classico, rispettivamente dovuti a cause entropiche ed entalpiche. Il primo é il responsabile della scarsa solubilitá e auto aggregazioni di oli e idrocarburi in acqua. Se mettiamo dell'olio di semi o esano in acqua vediamo che non si scioglie per niente e che si aggrega spontaneamente in gocce sulla superficie dell'acqua. Dalle misure sperimentali si ha, che il deltaG per il trasferimento di una molecola di butano in acqua é positivo e pari a:
deltaG = deltaH - TdeltaS = +24.5 kJ/mol
se prendiamo i termini singolarmente abbiamo:
deltaH = -4.3 kJ/mol
-TdeltaS = +28.7 kJ/mol
notiamo che in termini entalpici ci sarebbe un legame abbastanza forte da tenere insieme la molecola di butano con l'acqua ma tutto é annullato dall'altro termine: un -TdeltaS positivo vuol dire che il solo termine entropico é negativo, quindi c'é un effetto ordinante che sfavorisce il processo. Da dove viene ? Chi é che si organizza ? E' l'acqua. Le molecole di butano provocano un effetto detto di freezing sulle molecole della 1a sfera di solvatazione, cioé queste assumono una struttura tipo ghiaccio per compensare la rottura della struttura dell'acqua liquida dovuta alla presenza del butano. Piú lunga é la catena idrocarburica piú é grande la superficie esposta e di conseguenza l'effetto di freezing. E' per questo motivo che oli e idrocarburi in acqua si aggregano, in modo da ridurre la superficie esposta.
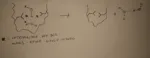
L'effetto idrofobico non classico invece avviene in strutture cavitose ed é basato su motivi entalpici. Lo possiamo riassumere con questa espressione: “ la cacciata dell’acqua “. Le spieghiamo meglio però con un esempio. Ammettiamo di avere una proteina con una cavità in cui due catene laterali di leucina sono separati fra loro da due molecole d’acqua. Le molecole d’acqua si interpongono fra i due residui con una interazione di van der Waals molto debole ( dipolo – dipolo indotto ). Come processo spontaneo avviene che la proteina si ripiega su sè stessa avvicinando i due residui e cacciando fuori l’acqua. E’ un processo entalpicamente guidato perchè le interazioni della situazione finale, legame a idrogeno fra le due molecole d’acqua, e la van der Waals fra i due residui, sono più forti rispetto alla situazione iniziale. Vi è anche un contributo entropico dovuto al fatto che dentro la cavità l’acqua è ordinata mentre una volta cacciata è disordinata nel solvente con un complessivo aumento di entropia.
Vi ringrazio dell'attenzione, spero di essere stato d'aiuto.
I seguenti utenti ringraziano zodd01 per questo messaggio: ohilà, NaClO, RhOBErThO, luigi_67, Claudio, Adriano, ClaudioG., Mercaptano