Organica-lover
2011-04-21 12:31
Preparazione della 2-amminobenzaldeide
Questa preparazione comporta la riduzione della 2-nitrobenzaldeide con solfato ferroso.
Si ottiene 2-amminobenzaldeide, che è profumata
MATERIALI OCCORRENTI:
-Pallone da 250ml
-bagnomaria
-refrigerante
-raccordo a T
-beuta da 100ml
-Buchner
-beuta codata
-pompa da vuoto
- FeSO4 eptaidrato
-HCl 1M
-1g 2-nitrobenzaldeide
-ammoniaca NH3
Modalità operativa:
In un pallone da 250ml si versano 60ml di acqua, 17,5g di FeSO4 eptaidrato e 1 ml di HCl 1M.
Si agita per sciogliere il solfato. Quindi si versa nel pallone 1g di 2-nitrobenzaldeide e 10ml di NH3 concentrata.
Si riscalda per 10 minuti a 80°C e si distilla raccogliendo 40ml di distillato. Si raccoglie su Buchner il composto odoroso(p.f. 38-39°C).
Dott.MorenoZolghetti
2011-04-22 12:01
Da dove lo tiri fuori il "composto odoroso"?
Sembrano le ricette di cucina di mia zia Gertrude. Caratteristica della cara zia: non ha mai cucinato in vita sua!
In effetti, spendere due parole sui meccanismi di reazione e utilizzare una terminologia più appropriata non farebbe male...
Infatti, non si capisce, il "composto odoroso" dove dovrebbe formarsi?
la riduzione di aldeidi aromatiche ad opera di sali di Fe(II) o Sn(II) è una buona alternativa all'uso di catalizzatori al Pd o Pt supportati su carbone e all'idrogeno gassoso, ma non è sempre attuabile.
ci sono alternative interessanti a seconda dell'uso e della stabilità del composto...
lungi da me far una lezione di chimica organica... ma ho scoperto che l'ammonio formato è un ottimo sostituto dell'idrogeno e sempre più spesso metodi "hydrogen-free" vengono sviluppati...
addirittura si può usare l'esotico SmI2
tornando a noi... il Fe(II) così come lo Sn(II) sono ottimi riducenti, e si ossidano istantaneamente a Fe(III) e Sn(IV) riducendo così il gruppo nitro a gruppo amino... con rese sufficienti allo scopo
probabilmente si tratta di SET (single electron transfert) da parte del catione metallico al nitrocomposto...
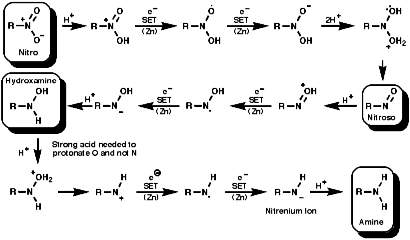 spero sia chiaro che non si va mai direttamente da nitro ad amino... ci sono step intermedi come il nitroso composto e l'idrossilamino composto
spero sia chiaro che non si va mai direttamente da nitro ad amino... ci sono step intermedi come il nitroso composto e l'idrossilamino composto
I seguenti utenti ringraziano quimico per questo messaggio: ale93, Organica-lover
Organica-lover
2011-04-22 17:54
grazie quimico!!...come sempre non potevi essere più chiaro di così.
doc e ale93...dopo che l'ho raccolto su buchner il composto aveva un odore di carattere lievemente agrumato.
...forse questo può darvi qualche delucidazione in più:
Nella famiglia delle aldeidi rientrano tutte quelle molecole, di origine organica, che rispondono alla
formula generica CnH2nO e che, nella loro struttura, mostrano il gruppo funzionale aldeidico –CHO.
Da un punto di vista chimico le aldeidi sono molecole abbastanza solubili in acqua, questo grazie al gruppo carbonile –C=O poco polare, sufficiente tuttavia a creare dei legami a idrogeno mediamente deboli se l’aldeide conserva una bassa massa molecolare.
Questa particolare categoria di molecole è facilmente ottenibile attraverso l’ossidazione, o
deidrogenazione, di un alcol primario, reazione cha avviene in presenza di dicromato di potassio.
A livello odoroso, invece, tali molecole sono conosciute per il la loro forte fragranza. Si parla
soprattutto di molecole lineari, piuttosto corte e alifatiche, ovvero a catena aperta, quando ci si
riferisce ad una fragranza aldeidica: le aldeidi che comprendono fra i nove e i dodici atomi di
carbonio, infatti, sono le classiche rappresentanti di quella che gli esperti del settore chiamano “nota
aldeidica”, un odore molto forte, con alcune qualità specifiche che gli donano caratteristiche
lievemente grasse e altrettanto delicatamente agrumate. In genere le aldeidi richiamano odori
naturali che appartengono a fiori o frutti, ma più raramente possono rispecchiare profumazioni
legnose o balsamiche; complessivamente si rivelano odori piacevoli, eppure la loro intensità e
aggressività spesso li rendono insopportabili.
E’ interessante notare come al variare del numero di atomi di carbonio presenti nella catena, anche
l’odore di queste molecole si modifichi: col diminuire di questi atomi in un numero compreso fra
otto e cinque, la profumazione assume sempre più un carattere agrumato; al contrario, con
l’aumentare della lunghezza della catena oltre le dodici unità di carbonio, l’odore si fa sempre più
grasso inizialmente, finendo poi nel ceroso.
La possibilità di imitazione degli odori della natura da parte di sostanze chimiche di sintesi era già
nota ai chimici agli inizi del XIX secolo; è proprio attorno a questi anni, e più precisamente nel
1826, che l’italiano Luigi Chiozza riprodusse, esclusivamente in laboratorio, il primo odore naturale
rappresentato proprio da un’aldeide: l’odore della cannella, portato dall’aldeide cinnamica. Ma
queste molecole dovettero aspettare quasi un secolo, prima di essere utilizzate in quantità rilevanti in un composto d’alta profumeria.
p.s. l' odore...adesso che ci penso, è simile a quello della citronella
Max Fritz
2011-04-22 18:26
La 2-aminobenzaldeide può essere detta anche antranilaldeide, e forse questa seconda nomenclatura (sicuramente meno corretta) richiama nella memoria dei chimici un'immagine molto più precisa. Infatti gli esteri dell'acido antranilico sono noti per il loro odore che ricorda gli agrumi e, a volte, l'essenza di fiori d'arancio.
Da ricordare anche, in fatto di aldeidi, l'aldeide C6, o n-esilaldeide o 1-esanale, utilizzatissima in profumeria per dare una nota di "verde", di prato appena tagliato e di fresco.
Organica-lover
2011-04-26 13:56
si...ci sono molte sostanze utilizzate in profumeria... il trans-2-esenale anche è molto utilizzato per una nota erbacea, il cis,cis-2,6-nonadiene-1-ale è utilizzato per dare l' odore di cocomero  ...la cinnamaldeide dall' odore di cannella... versalide per l' odore di muschio...il β- damascenone per l' odore di fragola....ecc..
...la cinnamaldeide dall' odore di cannella... versalide per l' odore di muschio...il β- damascenone per l' odore di fragola....ecc..
 spero sia chiaro che non si va mai direttamente da nitro ad amino... ci sono step intermedi come il nitroso composto e l'idrossilamino composto
spero sia chiaro che non si va mai direttamente da nitro ad amino... ci sono step intermedi come il nitroso composto e l'idrossilamino composto ...la cinnamaldeide dall' odore di cannella... versalide per l' odore di muschio...il β- damascenone per l' odore di fragola....ecc..
...la cinnamaldeide dall' odore di cannella... versalide per l' odore di muschio...il β- damascenone per l' odore di fragola....ecc..