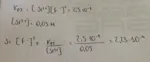Considerare una soluzione satura di SrF2:
a) calcolare la costante del prodotto di solubilità del sale sapendo che la concentrazione della soluzione satura è 8,6x10^-4 M;
b) calcolare la solubilità del sale in presenza di una concentrazione di F- pari a 0,05 M
Il primo punto l'ho risolto così:
È giusto? Ho qualche perplessità sul secondo punto.
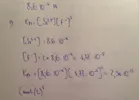 image.jpeg
image.jpeg
Nel calcolo della Ks c'è un errore di calcolo (per la legge di Murphy ci si accorge sempre degli errori degli altri e mai dei propri  ):
):
[F-] = 2 x 8,6·10^-4) = 1,72·10^-3 mol/L
perciò
Ks = 2,5·10^-9
Ti do due input per risolvere il secondo punto:
- la Ks resta uguale perché è una costante a temperatura costante
- la concentrazione totale di F- cambia
I seguenti utenti ringraziano LuiCap per questo messaggio: Mariù
Si infatti, è sempre così!  Perfetto, grazie! Allora provo a risolverlo e poi lo posto.
Perfetto, grazie! Allora provo a risolverlo e poi lo posto.
Ciao! Il secondo punto l'ho risolto così, ma immagino sia sbagliato.
Grazie, come sempre!
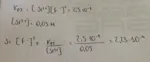 image.jpeg
image.jpeg
Sì, il procedimento che hai eseguito è sicuramente sbagliato.
A me risulta che la solubilità di SrF2 in una soluzione di F- 0,05 M diventa di 4,0·10^-4 mol/L, cioè diminuisce rispetto alla solubilità in acqua.
Se hai i risultati dell'esercizio, corrisponde?
Non ho risultato, come hai fatto? E comunque avevo sbagliato a scrivere la traccia. La concentrazione si riferisce a Sr2+, non F.
Grazie come sempre Luisa.
Se l'eccesso è di Sr2+ e non di F- cambia tutta la risoluzione dell'esercizio 
Il procedimento è questo:
 Mariù 2.jpg
Mariù 2.jpg
I seguenti utenti ringraziano LuiCap per questo messaggio: Mariù
Trascurando s come ho indicato, l'espressione della Ks diventa:
2,5x10^-9 = 0,05 x 4s^2 = 0,2s^2
I seguenti utenti ringraziano LuiCap per questo messaggio: Mariù
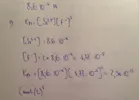
 ):
): Perfetto, grazie! Allora provo a risolverlo e poi lo posto.
Perfetto, grazie! Allora provo a risolverlo e poi lo posto.