La grande stabilità dello ione perclorato ha sempre precluso ai chimici molte delle classiche metodiche analitiche.
La simmetria tetraedrica dovuta alla disposizione degli elettroni di valenza che l'atomo centrale di cloro condivide con quella dei 4 di ossigeno è alla base di questa stabilità. Fatto è che solo pochi reagenti sono in grado di ridurre lo ione perclorato in modo controllato e riproducibile. Tra questi ricordiamo il Ti+++ (ma anche il V++, V+++,Cr++ e Mo+++) in soluzione acida, tutti capaci di ridurre il perclorato a ione cloruro. Sfortunatamente nessuno di questi reagenti è normalmente nella disponibilità di un homelab e comunque bisogna sempre lavorare in atmosfera esente da ossigeno.
A dire il vero una possibilità sarebbe quella della riduzione a secco nel crogiolo di Pt in presenza di cloruro di ammonio e calore. L'eccesso di sale ammoniacale è facilmente eliminabile e rimarrebbe solo un residuo del cloruro alcalino. Purtroppo si ha contemporaneamente una certa corrosione delle pareti interne e questo, innoquo per la precisione del metodo, non lo è per le tasche dell'analista. Come se non bastasse i perclorati sono decisamente refrattari in quanto a formare complessi di qualsiasi natura.
La tecnica gravimetrica sembra offrire qualche possibilità, ma solo alcuni metalli alcalini (K,Rb e Cs) hanno solubilità così basse da rendere fattibile la cosa. Ci sono poi alcuni composti organici come il Nitron e AsPh4Cl che formano sali molto poco solubili, ma oltre ad essere poco specifici sono anche costosi e di difficile reperibilità.
Sembrerebbe che per i comuni chimici dilettanti ogni via sia preclusa e invece esiste un reattivo capace di riuscire allo stesso tempo di facile reperibilità, poco costoso e abbastanza specifico. Non è molto sensibile ma uesto non è certo il pegiore dei mali.
Principio del metodo:
il meccanismo non è noto con precisione, tuttavia non è difficile ipotizzare che nella reazione tra certi coloranti organici basici con azoto terziario nella molecola e perclorati si formi un associato ionico insolubile, fortemente colorato e ben cristallizzato ie questo grazie anche alla voluminosità della molecola organica e la presenza di ioni zinco.
Reagenti:
- reattivo A: in un piccolo beker introdurre 2,5 g di zinco solfato eptaidrato e 2 g di potassio nitrato assieme a 20 ml di acqua distillata. Agitare con ancoretta magnetica fino a completa dissoluzione.
- reattivo B: soluzione acquosa di blu di metilene (CAS n° 122965-43-9) allo 0,03%
Esecuzione del test:
In un piccolo vetro d’orologio depositare 2 gocce del campione (soluzione neutra, evitare soluzioni acide) e 4 gocce del reattivo A. Aggiungere 2 gocce del reattivo B a fianco e poi unire le due soluzioni. Con movimenti del vetro mescolare bene. In presenza di perclorati si formano aghi finissimi di colore blu-viola. Al microsopio (da 20 a 50X) si notano aghetti finissimi che facilmente si aggregano in ciuffi. Per picole quantità occorre aspettare parecchi minuti.

A partire da sinistra: 1000 ppm di perclorato, 500 ppm e 0 ppm
Nota: in linea teorica sarebbe fattibile anche una determinazione spettrofotometrica del blu di metilene rimasto in soluzione. Come infatti appare evidente dalla fotografia l'intensità del colorante in soluzione è inversamente proporzionale al contenuto di perclorati.
Osservati sotto il microscopio polarizzatore, si evidenzia un notevole pleocromismo dei cristalli (vedi foto seguente)
http://www.imagestime.com/show.php/991002_ClO4BMpleoch..jpg.html
Sensibilità:
come già detto non è una reazione sensibilissima. In condizioni ideali si riescono ancora ad identificare con sicureza 500 ppm di perclorato
saluti
Mario
I seguenti utenti ringraziano Mario per questo messaggio: ohilà, fosgene, Beefcotto87, Roberto, Dott.MorenoZolghetti, zodd01, luigi_67, quimico, ClaudioG.
al-ham-bic
2014-11-27 22:54
Di tutte queste "strane" reazioni, di questi metodi analitici, di certe bellissime sintesi, quello che mi affascina, o meglio che mi affascinerebbe, non è tanto il metodo in sè (utile, meno utile, eccezionale... eccetera), quanto la sua "storia".
Nella fattispecie (ma gli esempi sono innumerevoli quanto le procedure stesse della chimica sperimentale) mi può andar bene la spiegazione ipotizzata.
-Ma, per esempio mi chiedo, perchè proprio una manatona di "zinco"?
-Zinco perchè era lì e costa poco (e magari funzionano anche cadmio o altri cationi) o perchè c'è un bello specifico motivo proprio per lui?
-Perchè abbiamo aggiunto proprio il salnitro?
-Come supporto di "potassio" o per una forte e prevista ragione? KNO3, dixit!
-Che età ha questa procedura per i perclorati?
-Chi è l'autore?
-Come avrà operato?
-Quanto di cui sopra (cioè di tutta la procedura) sarà stato frutto di un preciso "ragionamento" e quanto di una serie di, chiamiamole così, sperimentazioni "empiriche"?
Non si travisi in senso negativo questo termine!!! Il mondo è pieno di sperimentazioni empiriche che hanno portato a risultati eccezionali. Il difficile è ammetterlo a posteriori... (E' anche chiaro che il ragionamento deve sempre esserci e che per sperimentazioni empiriche non intendo dire lavorare "a caso" .
.
- Eccetera...
Tantissimi perchè che ovviamente non possono avere risposta (anche se talvolta le vie di Mario sembrano essere infinite...) e che per me sarebbero le cose più stuzzicanti ed interessanti, al di là delle convenienze pratiche di un metodo.
Di qualsiasi procedura, i suoi retroscena insomma.
Ma è fin troppo evidente che chiedo troppo e ho detto così per dire (ed anche perchè non mi piacciono le belle procedure lasciate senza commenti).
Ho usato apposta i due verbi chiave del discorso al condizionale.
Grazie e saluti anche da parte mia.
I seguenti utenti ringraziano al-ham-bic per questo messaggio: fosgene, quimico
Il tuo ragionamento al è interessante. E anche io, da ignorante chimico quale sono, a volte mi chiedo come siano arrivati ad un saggio o un'analisi particolare. Sicuramente prima i Chimici erano più smanettoni  e non avendo strumenti con la spina
e non avendo strumenti con la spina  dovevano arrangiarsi. Magari sapessi anche io al giorno d'oggi arrangiarmi
dovevano arrangiarsi. Magari sapessi anche io al giorno d'oggi arrangiarmi  sarei un chimico migliore, penso.
sarei un chimico migliore, penso.
Detto questo, a volte davvero, le vie di Mario sono infinite e ringrazio ogni giorno di poter imparare da lui, da te, da Moreno e da chiunque possa ampliare il mio bagaglio culturale.
Ormai non riesco ad immaginare la mia vita senza chimica...
Dott.MorenoZolghetti
2014-11-28 15:40
La storia della chimica analitica sperimentale ha un fascino tutto suo, è vero!
Tuttavia vorrei salvare Quimico da questo "pantano cognitivo": queste metodiche servono ben a poco, se uno dispone di strumenti moderni. Lo dico con tutto il rispetto, visto che spesso e volentieri andiamo a ripescare metodiche surclassatissime. Diciamo che alcune funzionano benino, altre sono sufficientemente complesse da giustificare il loro oblio. A un chimico moderno, me lo si lasci dire, è necessario conoscere tecniche strumentali complesse, non metodiche stantie. Quimico, come ben sai, per i perclorati basta una banale cromatografia ionica e sei tranquillo. 
Anche a me, come ad Al, garbano tantissimo le "cose vecchie" e per fortuna c'è qualcuno di buona volontà e di grande esperienza, che ce le illustra.
Ritornando sul discorso, ricadendo nel passato, trovo molto interessante la metodica che sfrutta il nitron per la ricerca dello ione nitrato, così come per quella dello ione perclorato e credo anche clorato. Qualcuno l'ha mai provata e ne conosce la procedura?
I seguenti utenti ringraziano Dott.MorenoZolghetti per questo messaggio: quimico, Mario
Ah beh certo, a me hanno farcito la testa di analitica STRUMENTALE e infatti io conosco bene quella. Non che non sappia altre tecniche non strumentali, ci mancherebbe.
Però, ci stanno anche queste, seppur vecchie, obsolete, surclassate e spesso assai complesse 
Anche a me garbano le cose vecchie... Hanno un loro enorme fascino.
Io attendo di leggerne di nuove 
A quanto vedo sono in parecchi, tra i lettori del forum, ad apprezzare le vecchie pratiche analitiche del passato. Ad una prima e sommaria occhiata sembrerebbe un diletto per nostalgici senza alcun fine pratico. Eppure, in un mondo dominato da metodiche strumentali, trovo che sia ancora appagante riuscire ad identificare questa o quella molecola con mezzi modesti e a misura umana. E poi quanti spunti si possono cavar fuori indagando sul come e perchè di quella reazione. Si rischia (ma è un vero piacere) di passare ore ad indagare su fenomeni altamente stimolanti per un chimico curioso.
Leggendo i commenti, c'è chi vorrebbe conoscere i retroscena e il percorso che ha portato ad elaborare un certo reagente.
Non sempre la cosa è possibile in quanto non ho accesso a tutta l'enorma massa di lavori pubblicati.
Però in questo caso ho qualche supplemento informativo.
Il blu di metilene era da tempo utilizzato in microscopia come colorante. Ben presto ci si accorse che in presenza di certe sostanze, anch'esse usate nella preparazione dei vetrini, questo colorante formava dei precipitati. L'elenco è piuttosto numeroso e annoverava, tra quelli formanti precipitati bluastri, il cloruro di zinco, il calomelano, i cloroplatinati, i molibdati e i ferrocianuri.
Proprio con il cloruro di zinco dà un sale doppio e in questa forma era solitamente commercializzato. Però le sue soluzioni non erano soddisfacenti e fornivano risultati incostanti per cui si pensò di usare altri sali di zinco al posto. Si vide inoltre che saturando la soluzione con sali (meglio di tutti quelli a base di nitrato) il precipitato era ancora più insolubile. Ecco in breve la genesi del reattivo. Va detto che anche usando una soluzione di blù di metilene si ha egualmente un precipitato, solo che la sensibilità è inferiore.
La formulazione del reattivo giunta a noi la si deve al lavoro di F. L. Hahn, Z. in "Angew. Chem., 39, 451-4 (1926)".
Ma il reagente non era solo una mera curiosità di laboratorio e infatti aveva usi pratici assai importanti per il tempo.
Veniva usato per testare la formazione dei perclorati durante il processo elettrolitico di preparazione. Era allora di notevole importanza conoscere quando e come procedeva l'ossidazione elettrochimica.
Monitorare la presenza dei perclorati come impurità nei nitrati aveva grande rilevanza per motivi opposti: negli esplosivi a base di nitrati la sua presenza poteva essere causa di instabilità e inoltre causava la precoce corrosione, per via dei gas corrosivi che si sviluppavano al momento della deflagrazione, alle pareti interne delle bocche da fuoco. Poi si scoprì che il nitro del Cile, allora usato come fonte di azoto nei fertilizzanti, ne conteneva quantità non trascurabili, cosa che aveva ripercussioni nel mondo vegetale e di conseguenza, anche alimentare.
saluti
Mario
I seguenti utenti ringraziano Mario per questo messaggio: fosgene, al-ham-bic, quimico, Dott.MorenoZolghetti
Dott.MorenoZolghetti ha scritto:
....................
Anche a me, come ad Al, garbano tantissimo le "cose vecchie" e per fortuna c'è qualcuno di buona volontà e di grande esperienza, che ce le illustra.
Ritornando sul discorso, ricadendo nel passato, trovo molto interessante la metodica che sfrutta il nitron per la ricerca dello ione nitrato, così come per quella dello ione perclorato e credo anche clorato. Qualcuno l'ha mai provata e ne conosce la procedura?
Moreno,
non ho mai avuto occasione di provare il Nitron.
Non si può avere tutto in un home lab. Bisogna farsene una ragione e così preferisco acquistare reagenti meno costosi e maggiormente utili.
Non che il Nitron non lo sia, ma per i nitrati e i perclorati esistono metodiche alternative a mio avviso maggiormente performanti.
E pensare che di questo reagente ho la procedura per sintetizzarlo e i prodotti necessari non sono poi nemmeno difficili da reperire.
P.S. la procedura per i nitrati è sopratutto gravimetrica. Questi vengono precipitati da una oluzione debolmente solforica all'ebollizione con una soluzione acetica del reattivo. Dopo raffreddamento in bagno ghiacciato si filtra su Gooch lavando con acqua freddissima. Si essicca a 110 °C fino a costanza di peso. Il nitrato di nitron contiene il 17,25 % di HNO3.
Purtroppo il metodo non è specifico in quanto sono molti gli anioni che nelle stesse condizioni precipitano: ossalati, ioduri e bromuri, perclorati, fluoborati.
saluti
Mario
I seguenti utenti ringraziano Mario per questo messaggio: Dott.MorenoZolghetti, quimico
Dott.MorenoZolghetti
2014-11-29 13:44
Condivido pienamente la riflessione di Mario: c'è sempre da imparare, anche da vecchie metodiche. Magari non servono per il lavoro, ma certamente servono per il sapere personale. E sono stimolanti, a volte anche molto.
Sul nitron, anch'io ho avuto lo stesso problema: costa molto e serve a poco, almeno rispetto ad altre procedure analitiche. Tuttavia mi è rimasta la curiosità e me ne voglio procurare un po'. Poi ne parleremo.
Per sintetizzarlo, ammettendo di saperlo fare, non avrei il tempo. Purtroppo.
I seguenti utenti ringraziano Dott.MorenoZolghetti per questo messaggio: quimico
I carbeni N-eterociclici (NHCs) sono reagenti estremamente utili in sintesi e catalisi, ma sfortunatamente sono molto costosi, tanto che in alcuni casi 1g arriva a costare diverse centinaia di euro (o dollari americani  ).
).
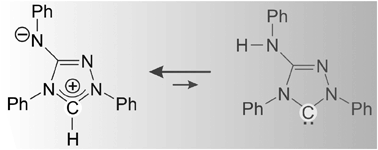
Comunque, come Ulrich Siemeling ed i suoi colleghi riportano nel loro articolo apparso su ChemComm, questo NHC sembra sia un'alternativa molto meno costosa per il futuro
Il team di scienziati dell'University of Kassel ha scoperto che il Nitron, un reagente analitico poco costoso, esibisce una sorprendente reattività quale carbene N-eterociclico, più affine al quella della sua forma tautomerica rispetto alla sua convenzionale struttura di Lewis. Facendo reagire il Nitron con dei tipici reagenti in grado di intrappolare i carbeni come zolfo elementale, CS2, e complessi di rodio, essi hanno dimostrato che è infatti il tautomero del Nitron che è responsabile per la sua reattività tipo-NHC in soluzione, sebbene sia presente a concentrazioni non determinabili tramite spettroscopia NMR.
Sono certo che diventerà presto una ottima scelta nelle reazioni degli NHC.
Nitron: a stable N-heterocyclic carbene that has been commercially available for more than a century - Christian Färber, Michael Leibold, Clemens Bruhn, Martin Maurer and Ulrich Siemeling, Chem. Commun., 2012,48, 227-229
I seguenti utenti ringraziano quimico per questo messaggio: fosgene


 .
. e non avendo strumenti con la spina
e non avendo strumenti con la spina  sarei un chimico migliore, penso.
sarei un chimico migliore, penso.