valeg96
2019-04-24 18:40
L'acido solfammico, sul quale si bisticciò un decimo di secolo fa con non poca confusione qui e https://www.myttex.net/forum/Thread-La-Saga-Dei-Solfammatiqui, è a tutti gli effetti un acido inorganico poco utile, se non per la sua baldanzosa acidità ( pKa = 1 ) e l'essere un anione relativamente grande*. Grazie anche alla sua solubilità, e alla solubilità dei suoi sali metallici, è usato specialmente in galvanotecnica, all'interno di miscele proprietarie per nickelatura o altri trattamenti, e per disincrostare superfici delicate che non possono essere trattate con acidi minerali forti. E' un prodotto molto economico (sui 10€/kg al dettaglio) ed è innocuo con le dovute riserve. Si produce per reazione di urea, SO3 ed acido solforico. In laboratorio può essere usato anche come standard per le titolazioni acido-base, se debitamente essiccato in stufa.
* L'esaammino cobalto (III) solfammato è un complesso di coordinazione molto facile da preparare, del quale forse parleremo in futuro.
Una delle sintesi più semplici dello Schlessinger, un magnifico manuale di sintesi inorganiche, è quella dei solfammati di Ba, Co, Ni e Cu [Sintesi 31 e 31a, p. 39-40]. In questo thread esporrò le sintesi dei sali di Co, Ni e Cu. Ho provato la sintesi del solfammato di Mn, ma con scarsi risultati che non vale la pena riportare. La sintesi del solfammato di Fe(II) è anch'essa fattibile, ma essendo il solfammato ferroso un forte riducente, è più impegnativa.
Reagenti:
Carbonato di rame, carbonato di nickel o carbonato di cobalto, qualche grammo ![[Irritante]](images/irritante.png.pagespeed.ce.KZwWJmvAGL.png) Può andare bene anche l'idrossido fresco.
Può andare bene anche l'idrossido fresco.
La resa è calcolata sul secondo reagente: acido solfammico seccato in stufa, circa 5 g ![[Corrosivo]](images/corrosivo.png.pagespeed.ce.CTVEf8LXM3.png)
Acqua distillata
Acetone >98% e/o Etanolo al 96% ![[Infiammabile]](images/infiammabile.png)
Procedimento:
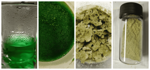
A circa esattamente 5 g di acido solfammico ben secco sciolto in 50 mL di acqua deionizzata si agigunge, sotto agitazione, il carbonato metallico a poco a poco. Quando cessa l'effervescenza si filtra la soluzione su Buchner per rimuovere il carbonato indisciolto ed eventuali impurezze ferriche. Al filtrato si aggiunge un cristallo (o una piccola punta di spatola) di acido solfammico e lo si evapora su piastra fino a consistenza oleosa. L'olio così ottenuto viene messo in stufa, o lasciato su bagnomaria, fin quando non solidifica. Il prodotto viene raccolto e tritato con acetone o etanolo al 96% (solo per Cu e Ba). Il prodotto finale viene essiccato in stufa a 100-120°C per svariate ore.
La resa è quantitativa.
I seguenti utenti ringraziano valeg96 per questo messaggio: ClaudioG., EdoB, FLaCaTa100, luigi_67, AminewWar, NaClO, ohilà, Geber